下列实验装置能达到相应实验目的是
| A.用图1装置制取Fe(OH)2沉淀 |
| B.用图2装置吸收NH3,并防止倒吸 |
| C.用图3装置蒸干AlCl3饱和溶液制备AlCl3晶体 |
| D.用图4装置比较Na2C03与NaHC03的稳定性 |
在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液生成沉淀的量与滴入NaOH溶液的体积关系如图所示则原混合溶液中Al2(S04)3与MgSO4的物质的量浓度之比为
| A.6:1 | B.3:1 | C.2:1 | D.1:2 |
若在能溶解氧化铝的溶液中,分别加入下列各组离子,可能大量共存的是
| A.NH4+、NO3-、 CO32-、 Na+ |
| B.NO3-、 Ba2+、K+、 Cl- |
| C.Al3+、Ba2+、Mg2+、HCO3- |
| D.NO3-、 K+、SO32-、 H+ |
NA表示阿伏加德罗常数。下列说法正确的是
| A.7.8 g Na2O2中含有的阴离子数目为0.2 NA |
| B.标准状况下,2.24 L CHCl3的分子数为0.1 NA |
| C.1 L 0.1 mol/L Al2(SO4)3溶液中,Al3+的数目为0.2 NA |
| D.9.2 g NO2和N2O4的混合气中含有的氮原子数为0.2 NA |
N2O5是一种新型硝化剂,在一定温度下可发生下列反应:2N2O5(g) 4NO2(g)+ O2(g) △H >0 ,T1温度下的部分实验数据为
4NO2(g)+ O2(g) △H >0 ,T1温度下的部分实验数据为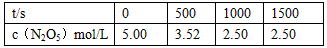
下列说法不正确的是
| A.500s内N2O5分解速率为2.96×10-3 mol/(L·s) |
| B.T1温度下的平衡常数为K1=125,1000s时转化率为50% |
| C.其他条件不变时,T2温度下反应到1000s时测得N2O5(g)浓度为2.98 mol/L,则T1<T2 |
| D.T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1 >T2,则K1> K2 |
已知某反应中反应物与生成物有:KIO3、Na2SO3、H2SO4、I2、K2SO4、H2O 和未知物X。下列说法中不正确的是
| A.该未知物X为Na2SO4 |
| B.该反应的氧化剂是KIO3 |
| C.该反应中,发生氧化反应的过程是KIO3→I2 |
| D.由反应可知还原性强弱顺序为:Na2SO3>I2 |