下表中所示物质或概念间的从属关系符合下图的是

| |
X |
Y |
Z |
| A |
钠元素 |
主族元素 |
短周期元素 |
| B |
氢氧化铁(固体) |
胶体 |
分散系 |
| C |
电解质 |
化合物 |
纯净物 |
| D |
置换反应 |
氧化还原反应 |
放热反应 |
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子说法正确的是
| A.含有碳碳双键、羟基、羰基、羧基 |
| B.含有苯环、羟基、醛基、羧基 |
| C.含有羟基、羰基、羧基、酯基 |
| D.含有碳碳双键、苯环、酯基、羰基 |
下列各组有机物只用一种试剂无法鉴别的是
| A.乙醇、甲苯、硝基苯 | B.苯、苯酚、己烯 | C.苯、甲苯、环己烷 | D.甲酸、乙醛、乙酸 |
下列各化合物的命名中正确的是
下列反应中,属于取代反应的是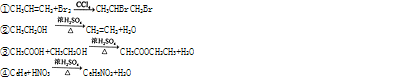
| A.①② | B.③④ | C.①③ | D.②④ |
已知C5H11Br有8种同分异构体,则C6H12O2属于羧酸的结构有(不考虑立体异构)
| A.4种 | B.6种 | C.8种 | D.16种 |