向某酸性透明溶液中加入新制氯水后,各离子仍可大量共存的是
| A.Fe3+、K+、SO42-、NO3- | B.K+、Na+、SO32-、Cl- |
| C.NH4+、K+、SO42-、Br- | D.K+、Na+、AlO2—、NO3— |
下列说法不正确的是()
| A.同温同压下,3 mol C2H2(g)和1mol C6H6(g)的密度相等 |
| B.非金属氧化物不一定是酸性氧化物,但大多数金属氧化物为碱性氧化物 |
| C.具有相同分子数的甲酸甲酯与乙酸的共价键数相等 |
| D.SO2、H2O2、活性炭都能使品红溶液褪色,但原理不同 |
把SO2通入Fe(NO3)3溶液中,溶液由黄色变为浅绿色,但立即又变为黄色,此时若滴入BaCl2溶液,则会产生白色沉淀.在上述一系列变化过程中,最终被还原的是
| A.SO2 | B.NO |
C.Fe3+ | D.Fe2+ |
Na2FeO4是一种高效多功能水处理剂,应用前景十分看好。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,对此反应下列说法中正确的是
| A.Na2FeO4既是氧化产物又是还原产物 |
| B.Na2O2只作氧化剂 |
| C.O2是还原产物 |
| D.2 mol FeSO4发生反应时,反应中共有8 mol电子转移 |
设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A.100 mL l mol·L-1的碳酸钠溶液中含有的CO32-数为0.1NA |
| B.71 g氯气被还原得到的电子数为2NA |
| C.标准状况下,2.24 L苯中含有的碳原子数为0.6 NA |
| D.用含有少量锌、铁、银等杂质的粗铜作阳极电解精炼,当阴极析出64 g金属时阳极失去的电子数小于2NA |
常温下,下列各组离子在指定环境下能大量共存的是()
A.pH=7的溶液中Al3+、Cl-、SO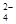 、HCO 、HCO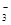 |
B.由水电离出来的c(H+)=10-12mol/L的溶液中Na+、HCO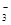 、SO 、SO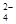 、K+ 、K+ |
| C.pH=0的溶液中Na+、K+、Fe2+、ClO- |
D.c(OH-)=10-2mol/L的溶液中S2-、SO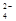 、S2O 、S2O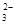 、Na+ 、Na+ |