工业制得的氮化铝(AlN)产品中常含有少量Al4C3、Al2O3、C等杂质.某同学设计了如下实验分别测定氮化铝(AlN)样品中AlN和Al4C3的质量分数(忽略NH3在强碱性溶液中的溶解).
(1)实验原理
①Al4C3与硫酸反应可生成CH4,
②AlN溶于强酸产生铵盐,溶于强碱生成氨气,请写出AlN与过量NaOH溶液反应的化学方程式 ,
(2)实验装置(如图所示)

(3)实验过程
①连接实验装置,检验装置的气密性.称得D装置的质量为yg,滴定管的读数为amL.
②称取xg AlN样品置于装置B瓶中;塞好胶塞,关闭活塞 ,打开活塞 ,通过分液漏斗加入稀硫酸,与装置B瓶内物质充分反应.
③待反应进行完全后,关闭活塞 ,打开活塞 ,通过分液漏斗加入过量 (填化学式),与装置B瓶内物质充分反应.
④ (填入该步应进行的操作).
⑤记录滴定管的读数为bmL,称得D装置的质量为zg.
(4)数据分析(已知:该实验条件下的气体摩尔体积为Vm L•mol﹣1)
①Al4C3的质量分数为 .
②若读取滴定管中气体的体积时,液面左高右低,则所测气体的体积 (填“偏大”、“偏小”或“无影响”).
③AlN的质量分数为 。
(8分)下面a~f是中学化学实验中常见的几种仪器:
a.量筒 b.容量瓶 c.托盘天平 d.温度计 e.分液漏斗
(1)标出仪器使用温度的是________(填写编号)。
(2)使用前需要检查是否漏水的是________(填写编号)。
(3)称取10.5 g固体样品(1 g以下使用游码)若样品与砝码错放位置,则实际称取的样品质量为________ g。
(4)配制2 mol·L-1 H2SO4时,用a量取浓H2SO4时视线高于液面,则配得的浓度(偏高、偏低或无影响)
如图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题: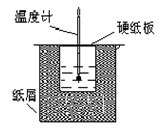
(1)从实验装置上看,图中伤缺少的一种玻璃仪器是_____________;
(2)烧杯间填满碎纸条的作用是____________________;
(3)若大烧杯上不盖硬纸板,求得的反应热数值__________(填“偏大”“偏小”或“无影响”)。
(4)实验中该用60 mL 0.50 mol·L-1HCl跟50 mL 0.55 mol·L-1 NaOH溶液进行反应,与上述实验相比,所放出的热量_________(填“相等”或“不相等”),所求中和热__________(填“相等”或“不相等”)。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会________(填“偏大”“偏小”或“无影响”)。
工业制纯碱时,第一步通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠结晶。它的反应原理可以用下面的方程式表示:
NH3+CO2+H2O==NH4HCO3,NH4HCO3+NaCl(饱和)==NaHCO3↓+NH4Cl
以上反应的总结果是放热反应。下面设计了一个实验,用最简单的实验装置模拟实验这一过程,获得碳酸钠结晶。可供选择的实验用品有:稀盐酸、稀硫酸、浓氨水、氢氧化钠、消石灰、石灰石、氯化铵、食盐、蒸馏水和冰,以及中学化学实验常用仪器。实验装置示意图(包括反应时容器中的物质)如下,图中玻璃容器旁自左至右分别用A、B、C……符号标明(请见题后说明)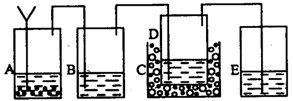
(1)请写出在图上A、B、C……各玻璃容器中盛放物质的化学式或名称。
A:__________________,B:___________________,C:__________________,
D:__________________,E_____________________。
(2)利用在本题所提供的实验用品,如何判断得到的产品是碳酸氢钠的结晶,而不是碳酸氢铵或食盐结晶?
实验室可以用下图装置进行CO还原赤铁矿(主要成分为Fe2O3)并测定其中铁的含量的实验(假设杂质不参加反应)。请回答下列问题: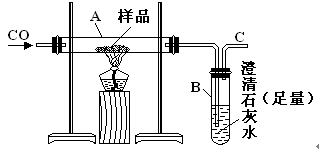
(1)该实验中炼铁的方法是填字母)。
| A.热分解法 | B.热还原法 | C.电解法 | D.湿法冶金 |
(2)实验开始后,B中的现象是。
A中有关反应的化学方程是。
(3)C处须进行尾气处理,其方法是。
(4)若样品的质量为3.6g,通入足量的CO充分反应后,B增重2.64g,则样品中铁的质量分数为(结果保留一位小数)。
海带中含有丰富的碘元素,某化学研究性学习小组用如下流程从海水中提取碘: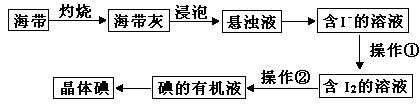
(1)若操作①为通入适量的Cl2,则发生反应的离子方程式为。
(2)操作②的名称是,所用的玻璃仪器有,可以选用的有机溶剂是(填一种)。