下列过程没有发生化学反应的是
| A.用食醋除去暖水瓶中的薄层水垢 | B.石油的分馏和煤的干馏 |
| C.用二氧化氯(ClO2)为自来水消毒 | D.液氨作制冷剂 |
进行下列实验,由实验现象得出的结论正确的是
| A.某气体能使湿润的淀粉KI试纸变蓝,该气体一定是Cl2 |
| B.向某溶液中滴加KSCN溶液,溶液显红色,该溶液中含有Fe3+ |
| C.向某溶液中逐滴滴加稀氨水至过量,先产生白色沉淀然后沉淀溶解,该溶液中含有Al3+ |
| D.向某溶液中通入CO2溶液变浑浊,继续通CO2浑浊消失,该溶液可能是Na2SiO3溶液 |
短周期主族元素X、Y、Z在元素周期表中的相对位置如图,下列推论合理的是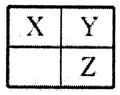
| A.若Z的核电荷数是Y的两倍,则X为碳元素 |
| B.若X、Y、Z的单质常温下都是气体,则Y为氧元素 |
| C.若X、Y、Z都是非金属元素,则它们气态氢化物的水溶液都显酸性 |
| D.若X、Y、Z的原子序数之和等于25,则它们都是非金属元素 |
设NA为阿伏加德罗常数的数值,下列叙述错误的是
| A.在1.8g18O2中含有NA个质子 |
| B.28gC2H4中含有4NA个C—H键 |
| C.常温下,2.7g铝片投入足量的稀硫酸中,铝失去的电子数为0.3NA |
| D.4.6gNa完全转化成Na2O和Na2O2的混合物,生成物中阴离子总数为0.1NA |
“玉兔号”巡月器的发动机套有一件“土豪金”外衣——耐高温、抗震复合材料,该复合材料以硅酸铝纤维(Al2O3—SiO2)为基体,六钛酸钾晶须(K2O·6TiO2)为增强剂。下列说法中正确的是
| A.该复合材料属于新型有机非金属材料 |
| B.Al、K、Ti都属于主族元素 |
| C.原子半径:K>Si>O |
| D.该复合材料能耐强酸和强碱腐蚀 |
根据原子结构及元素周期律的知识,下列推断正确的是
A.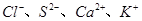 半径逐渐减小 半径逐渐减小 |
B.还原性强弱: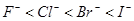 |
| C.核外电子排布相同的微粒化学性质一定相同 |
| D.同主族元素含氧酸的酸性随核电荷数的增加而减弱 |