常温下,向20 mL某浓度的盐酸中逐滴加入0.1 mol/L的氨水,溶液pH的变化与加入氨水的体积关系如图所示。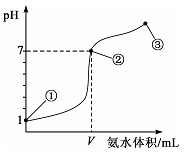
下列叙述正确的是
| A.盐酸的物质的量浓度为l mol/L |
| B.在①、②之间的任意一点:c(Cl-)>c(NH4+),c(H+)>c(OH-) |
| C.在点②所示溶液中:c(NH4+)=c(Cl-)>c(OH-)=c(H+),且V<20 |
| D.在点③所示溶液中:由水电离出的c(OH-)>l0-7mol/L |
水的电离平衡为H2O  H+﹢OH-,△H>0,下列叙述不正确的是( )
H+﹢OH-,△H>0,下列叙述不正确的是( )
| A.将水加热,pH减小 | B.恒温下,向水中加入少量固体KOH,Kw不变 |
| C.向水中滴入稀醋酸,c(H+)增大 | D.向水中加入少量固体NaClO,平衡逆向移动 |
在密闭容器中,反应X2(g) +Y2(g)  2XY(g);△H < 0,达到平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是.( )
2XY(g);△H < 0,达到平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是.( )
| A.图I是加入适当催化剂的变化情况 | B.图II是扩大容器体积的变化情况 |
| C.图III是增大压强的变化情况 | D.图III是升高温度的变化情况 |
如图,A池用石墨电极电解NaOH溶液,B池精炼粗铜,一段时间后停止通电,A池中D极产生具有氧化性的气体在标准状况下为2.24L。下列说法正确的是()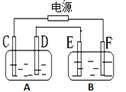
A.A池溶液的pH保持不变 B.D、E两极都发生氧化反应
C.E极应为粗铜板材料 D.B池中E极质量增加12.8g
下列说法正确的是()
| A.相同温度下,1 mol·L-1醋酸溶液与0.5 mol·L-1醋酸溶液中,c(H+)之比是2∶1 |
| B.向醋酸钠溶液中加入适量醋酸,使混合液的pH=7,此时混合液中c(Na+)=c(CH3COO-) |
| C.pH=3的盐酸和醋酸加水使溶液体积分别扩大100倍,pH仍相同 |
D.0.1 mol·L-1NH4Cl溶液中c( )+c(H+)=c(Cl-) )+c(H+)=c(Cl-) |
将4molSO2和2molO2充入2L的密闭容器中,在一定条件下发生反应,经2s后测得SO3的浓度为0.6mol·L-1,下列说法中正确的是()
①用O2表示的反应的平均速率为0.6mol·L-1·s-1
②用SO2表示的反应的平均速率为0.3mol·L-1·s-1
③2s时SO2的转化率为15%
④2s时O2的浓度为0.7mol·L-1
| A.①③ | B.①④ | C.②③ | D.②④ |