某工厂的废渣中混有少量的锌粉和氧化铜(其他成分不与酸反应),跟大量废盐酸接触形成污水,产生公害。若向污水中撒入铁粉且反应后铁粉有剩余,此时污水中一定含有的金属离子是( )
| A.Fe2+、Cu2+ | B.Cu2+、H+ | C.Zn2+、Fe2+ | D.Zn2+、H+ |
以下关于下图说法正确的是
| A.上图表明催化剂可以改变反应的热效应 |
| B.上图表示某反应能量的变化与生成物状态无关 |
| C.上图表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| D.上图表明化学反应不仅遵循质量守恒定律,也遵循能量守恒 |
下表是元素周期表一部分。X、Y、Z均为短周期元素,X、Z的质子数之和为23,下列说法正确的是
| A.W的原子序数比Z的大9 |
| B.Y的最高价氧化物溶于水,与水反应得到酸 |
| C.W的单质能与Z的一种氧化物的水溶液反应生成两种强酸 |
| D.Z的单质在一定条件下可与铁粉反应,将铁粉氧化为+3价 |
下述四个反应中,酸所体现的性质与其他三者明显不同的是
| A.浓盐酸与二氧化锰共热制氯气 |
| B.浓硫酸与铜片加热 |
| C.浓硝酸与铜反应 |
| D.稀硝酸与铜反应 |
水热法制备Fe3O4纳米颗粒的总反应: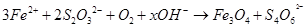
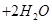 ,有关说法正确的是
,有关说法正确的是
| A.每转移1.5mol电子,有1.125mol Fe2+被氧化 |
| B.x=2 |
| C.Fe2+、S2O32-都是还原剂 |
| D.每生成1mol Fe3O4,转移电子2mol |
利用下列实验装置进行的相应实验,不能达到实验目的的是
| A.图1所示装置可制取氨气 |
| B.图2所示装置可分离CH3CH2OH和CH3COOC2H5混合液 |
| C.图3所示装置可制备Fe(OH)2并容易观察到白色沉淀 |
| D.图4所示装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂自性、还原性 |