甲醇是重要的化工原料,又可称为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g) CH3OH(g);△H1
CH3OH(g);△H1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g);△H2
CH3OH(g)+H2O(g);△H2
③CO2(g)+H2(g) CO(g)+H2O(g);△H3
CO(g)+H2O(g);△H3
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
| 化学键 |
H-H |
C-O |
CO的键能 |
H-O |
C-H |
| E/(kJ.mol-1) |
436 |
343 |
1076 |
465 |
413 |
由此计算△H1= kJ.mol-1,已知△H2=-58kJ.mol-1,则△H3= kJ.mol-1
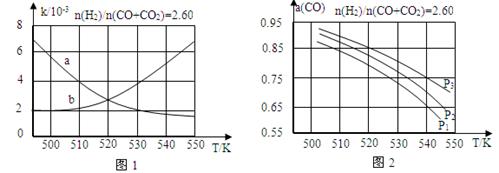
(2)反应①的化学平衡常数K的表达式为 ;图1中能正确反映平衡常数K随温度变化关系的曲线为 (填曲线标记字母),其判断理由是 。
|
在VmLFe2(SO4)3溶液中含Fe3+ m g,取该溶液V/4mL,加水稀释至4VmL,则此稀溶液中SO42—的物质的量浓度为。
27.2g某二价金属的氯化物ACl2中含有0.4mol Cl-离子,ACl2的摩尔质量是,A的相对原子质量是。
等质量的CuO和MgO粉末分别溶于相同体积的硝酸中,得到Cu(NO3)2和Mg(NO3)2溶液的浓度分别为amol/L和bmol/L,则a与b的关系为。
在标准状况下,H2、O2、N2和H2O四种物质各1 g,体积最小的是______。
某盐的无色溶液中同时有Cl-、SO42-,检验时,应先检验离子,首先取少量待测液于试管中,向其中加入试剂且至时,经过操作后,再用试剂检验另一种离子。