(1)已知:2Fe3++2I-===2Fe2++I2, 2Fe2++Br2===2Fe3++2Br-。
①根据以上方程式比较Fe2+、Br-、I-还原性的强弱
②含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此时被氧化的离子是________
(2)在硫酸铝、硫酸钾和明矾的1 L混合溶液中,如果SO42-浓度为0.4 mol/L,当加入等体积0.4 mol/L KOH溶液时,生成的沉淀恰好完全溶解,反应后混合溶液中K+的浓度为_______mol/L
某有机化合物A的结构简式如图20,回答下列问题:
⑴ A的分子式为 ;
⑵ A在NaOH水溶液中加热得到B和C,C是芳香族化合物,则C的结构简式为 ;
⑶ B与足量的某饱和一元羧酸D充分反应后生成E ,E和B的相对分子质量之差为84 ,则D的摩尔质量为 ;
⑷ C酸化后可得F,F不能发生的反应类型是(填字母代号) ;
a.取代反应b.加成反应c.消去反应
d.加聚反应 e.氧化反应 f.还原反应
⑸ F可以发生如图21的转化,且G与H互为同分异构体。请写出:
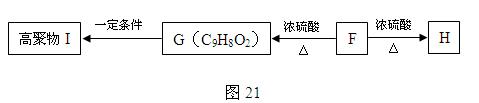
① H的结构简式 ;
② 由F生成G的化学方程式 ;
⑹ 符合下列三个条件的F的同分异构体共有 种。
① 含有邻二取代苯环结构 ② 与F具有相同的官能团
③ 不与FeCl3溶液发生显色反应
|
某研究性学习小组在CO还原Fe2O3的实验中,用磁铁吸出生成的黑色粉末X,他们认为X不一定是Fe,若温度不均时会生成Fe3O4,也能被磁铁吸引。为了探究X的组成,他们进行了如下实验。
I、定性检验
| 实验编号 |
实验操作 |
实验现象 |
| ① |
取少量黑色粉末X放入试管1中,注入浓盐酸,微热 |
黑色粉末逐渐溶解,溶液呈黄绿色,有少量气泡产生 |
| ② |
另取少量黑色粉末X放入试管2中,注入足量硫酸铜溶液,振荡,静置 |
有极少 量红色物质析出,仍有较多黑色固体未溶解 量红色物质析出,仍有较多黑色固体未溶解 |
由上述实验现象推断,黑色粉末X的成分是。
II、定量测定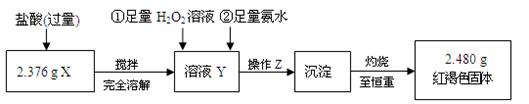
⑴ 操作Z的名称是,如图19的仪器中,在灼烧沉淀时必须用到的是(填字母)。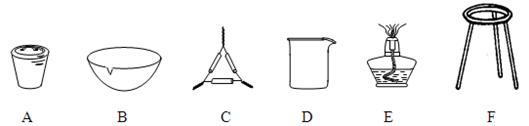
⑵ 写出溶液Y中滴加H2O2溶液时发生反应的离子方程式:
。
⑶ 将沉淀物加热,并置于干燥器中冷却至室温,用托盘天平称量其质量为b1 g,再次加热并冷却至室温称量其质量为b2 g,若b1- b2= 0.3 g,则接下来还应进行的操作是
。
⑷ 有同学认为:上述流程若不加入H2O2,其它步骤不变,只要在空气中充分放置仍可达到目的。他的理由是(用化学方程式表示):
。
⑸ 通过以上数据,得出2.376 g黑色粉末中各成分的物质的量为。
已知A、B为常见的金属单质,C、D为常见的非金属单质,甲、乙、丙为三种常见的化合物,甲是中学化学中常见的红棕色粉末状固体,它们之间的相互转化关系如图18所示(部分产物及反应条件没有列出):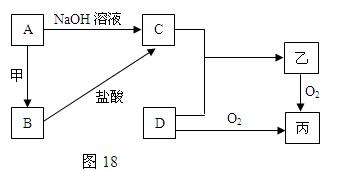
⑴ 写出框图中A转化为B的化学方程式:,该反应属于(填“吸热反应”或“放热反应”),引发该反应的操作是。
⑵ 若乙的水溶液呈弱酸性 ,丙是一种大气污染物、有刺激性气味。已知16 g固体单质D完全燃烧转化成丙时,放出148.4 kJ的热量,则该反应的热化学方程式为:
,丙是一种大气污染物、有刺激性气味。已知16 g固体单质D完全燃烧转化成丙时,放出148.4 kJ的热量,则该反应的热化学方程式为:
。
⑶ 若乙在水溶液中呈弱碱性,其盐可用作化肥,且C与D化合生成乙的反应是可逆反应。
① 将等物质的量的C、D两种单质充入一体积恒定的密闭容器中,在适当催化剂和恒温条件下反应,下列说法中不正确的是(填 字母)。
字母)。
a.达到化学平衡时,2 v正(C) = 3 v逆(乙)
b.反应过程中,D单质的体积分数始终为50 %
c.达到化学平衡时,混合气体的密度减小
d.达到化学平衡的过程中,气体的平均相对分子质量逐渐增大
e.达到化学平衡后,再升高温度,乙的体积分数增大
② 若在一个体积为10 L的密闭容器中,充入8 mol C单质和2 mol D单质,在一定温度下发生反应生成气体乙,经40 min后反应达到平衡,此时C的转化率为37.5 %。从反应开始到达平衡的40 min内,用物质乙表示的化学反应速率为;达到平衡后,若向容器中按5︰1︰2的物质的量之比再次充入C、D、乙三种物质,则原平衡体系中C的转化率将(填“增大”、“减小”或“不变”)。
A、B、C、D、E、F均为短周期元素,且原子序数依次增大,A是原子半径最小的元素,B的最高价氧化物的水化物可与其氢化物反应形成离子化合物甲;A与D可以按照原子个数比4︰1形成化合物乙,且乙分子中含有18个电子,E与B同主族,C的阳离子与F的阴离子相差一个电子层,且可形成离子个数比为2︰1的离子化合物丙。
⑴ D的原子结构示意图为,B单质的电子式为,E在周期表中的位置为;
⑵ 下列说法正确的有;
a.化合物乙为正四面体形分子,是由极性键构成的非极性分子
b.C、D、E、F原子半径由大到小的顺序为 C > D > E > F
c.B、E形成的氢化物中,B的氢化物稳定性更强,是因为该分子中存在氢键
d.化合物甲和化合物丙都含有离子键和共价键
⑶ 将F在空气中完全燃烧的产物通入BaCl2和HNO3的混合溶液,生成白色沉淀并放出无色气体,请用一个离子方程式表示该反应:
;
⑷ 写出一个由以上元素构成的10 e- 微粒与18 e- 微粒反应的离子方程式:
;
⑸ 在1 mol·L-1甲溶液中,下列关系式正确的是;
a.c(NO3-) > c(NH4+) > c(H+) > c(OH-)
b.c(NH4+) > c(NO3-) > c(H+) > c(OH-)
c.c(NO3-) = c(NH4+) > c(H+) = c(OH-)
d.c(NH4+) = c(NO3-) > c(H+) > c(OH-)
⑹ 25 ℃时,丙的水溶液的pH大于7,其原因是(用离子方程式解释):
。
某常见金属X,有下列关系图,其中A、B分别是X的正二价、正三价金属离子,请回答:
(1)写出X的名称,Y的化学 式。
式。
(2)写出下列反应的化学方程式或离子方程式:
① X和稀盐酸反应生成A和某种气体的离子方程式
② +2价的A被Y氧化反应生成+3价的B的离子方程式
③ X粉末和硫酸铜溶液发生置换反应的离子方程式
④ X的正三价氧化物(X2O3)和铝粉反应的化学方程式
(3)A溶液与NaOH溶液在空气中反应的现象 。
。
并写出有关的化学方程式。