在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如图所示,由此确定,原溶液中含有的阳离子是:
| A.Mg2+、Al3+、Fe2+ | B.H+、Mg2+、Al3+ |
| C.H+、Ba2+、Al3+ | D.只有Mg2+、Al3+ |
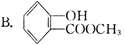
一定量的某有机物溶解于适量的NaOH溶液中,滴入酚酞试液呈现红色,煮沸5 min后溶液颜色变浅,再加入盐酸至酸性时,沉淀出白色晶体。取少量晶体放在FeCl3溶液中,溶液呈现紫色。该有机物可能是


下列各有机物在一定的条件下能发生消去反应的是()
| A.CH3Cl | B.(CH3)3CCH2OH | C.(CH3)3CCl | D.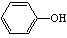 |
某有机物的结构简式为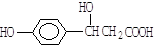 ,它可以发生的反应类型有
,它可以发生的反应类型有
(a)取代 (b)加成 (c)消去 (d)酯化 (e)水解 (f)中和 (g)加聚
| A.(a)(c)(d)(f) | B.(b)(e)(f)(g) | C.(a)(b)(c)(d)(g) | D.除(e)(g)外 |
下列反应中,属于取代反应的是
①CH3CH=CH2+Br2 CH3CHBrCH2Br
CH3CHBrCH2Br
②CH3CHO+2Ag(NH3)2OH 2Ag↓+CH3COONH4+3NH3+H2O
2Ag↓+CH3COONH4+3NH3+H2O
③CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
④C6H6+HNO3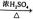 C6H5NO2+H2O
C6H5NO2+H2O
| A.①② | B.③④ | C.①③ | D.②④ |
目前工业上用乙烯制乙醛的过程分为三步进行:
①CH2=CH2+PdCl2+H2O → CH3CHO+2HCl+Pd
②Pd+2CuCl2= PdCl2+2CuCl
③2CuCl+1/2O2+2HCl=2CuCl2+H2O
对于整个生产过程,下列叙述正确的是
| A.CH2=CH2是还原剂,PdCl2是氧化剂 |
| B.CuCl是还原剂,O2是氧化剂 |
| C.乙烯是还原剂,O2是氧化剂 |
| D.Pd和CuCl都是催化剂 |