下列有关电化学原理的说法中,错误的是
| A.在现实生活中,电化学腐蚀要比化学腐蚀严重的多,危害更大 |
| B.在铜的精炼装置中,通常用粗铜作作阳极,精铜作阴极 |
| C.氯碱工业,主要依托电解熔融的氯化钠来制取工业上重要的化工原料烧碱和氯气 |
| D.可充电的电池称“二次电池”,在充电时,是将电能转变成化学能,在放电时,又将化学能转化成电能 |
由两种短周期元素构成的某常见离子化合物,阴阳离子所含的电子数不相等。关于该离子化合物的下列说法中正确的是( A )
①晶体中阴阳离子的数目之比一定是1:1
②两元素可以在同一周期也可在不同周期
③晶体内一定只有离子键没有共价键
④阴离子的电子数一定大于阳离子的电子数
| A.② | B.②④ | C.②③④ | D.①②③④ |
为确定某溶液的离子组成,进行如下实验:
①测定溶液的pH=13;
②取少量溶液加入过量稀盐酸,产生无刺激性、能使澄清石灰水变浑浊的气体;
③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀;
④取上层清液继续滴加Ba(NO3)2溶液至不再产生沉淀时,再滴加AgNO3溶液,产生
白色沉淀。
根据实验以下判断不正确的是( C)
| A.溶液中一定有CO32- |
| B.溶液中一定有SO42- |
| C.不能确定溶液中是否存在HCO3- |
| D.不能确定溶液中是否存在Cl- |
物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度等有关,下列各组物质:
①Cu与HNO3溶液 ②Fe与盐酸③Zn与H2SO4溶液 ④Cl2与FeCl2溶液
由于浓度不同而能发生不同氧化还原反应的是 ( C )
| A.①②③ | B.①③④ | C.①③ | D.①②③④ |
对现有元素周期表的下列说法中,正确的是( D )
A.主族都含有非金属元素 B.主族都含有金属元素
C.最外层电子数为2的都是金属元素 D.副族都是金属元素
设NA代表阿伏加德罗常数,以下说法正确的是
| A.标准状况下,22.4 L甲烷和氮气混合物所含的分子数为N |
B.常温常压下1 mol NO2气体与水反应生成NA个NO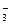 离子 离子 |
C.标准状况下,1 L水所含分子数为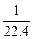 NA NA |
D.78 g Na2O2溶于水后所得溶液中含有O2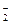 离子数为NA 离子数为NA |