已知反应:2NO2(g)+4CO(g) N2(g)+4CO2(g) ΔH<0。将一定量的NO2与CO充入装有催化剂的注射器中后封口。右图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法不正确的是
N2(g)+4CO2(g) ΔH<0。将一定量的NO2与CO充入装有催化剂的注射器中后封口。右图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法不正确的是

| A.b点的操作是快速压缩注射器 |
| B.c点与a点相比,c(NO2)、c(N2)都增大 |
C.e点: (正) < (正) < (逆) (逆) |
| D.若考虑体系温度变化,且没有能量损失,则平衡常数K(c) >K(f) |
已知B是常见的金属单质,E为常见的气态非金属单质,H常温下为无色液体,C的浓溶液在加热时才与D反应。根据下列框图所示,试回答: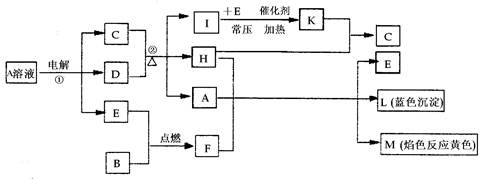
(1)F的电子式为,所含化学键为;
(2)反应①的离子方程式为;
(3)每生成1 mol K,反应放出98.3 kJ的热量,该反应的热化学方程式为;
(4)反应②的化学方程式为;
(5)化合物F与Na2S溶液反应,生成NaOH和S单质,试写出该反应的离子方程式为。
科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是 ( )
| A.分子中N、O间形成的共价键是非极性键 |
| B.分子中四个氮原子共平面 |
| C.该物质既有氧化性又有还原性 |
| D.15.2g该物质含有6.02×1022个原子 |
下列叙述中正确的是 ( )
| A.NH3、CO、CO2都是极性分子 |
| B.CH4、CCl4都是含有极性键的非极性分子 |
| C.HF、HCl、HBr、HI的稳定性依次增强 |
| D.CS2、H2O、C2H2都是直线型分子 |
下列事实与氢键有关的是()
| A.水加热到很高的温度都难以分解 |
| B.水结成冰体积膨胀,密度变小 |
| C.CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高 |
| D.HF、HCl、HBr、HI的热稳定性依次减弱 |
下列说法中正确的是()
| A.C60气化和I2升华克服的作用力相同 |
| B.甲酸甲酯和乙酸的分子式相同,它们的熔点相近 |
| C.氯化钠和氯化氢溶于水时,破坏的化学键都是离子键 |
| D.用作高温结构陶瓷材料的Si3N4固体是分子晶体 |