中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论正确的是
| 选项 |
规律 |
结论 |
| A |
较强酸可以制取较弱酸 |
次氯酸溶液无法制取盐酸 |
| B |
反应物浓度越大,反应速率越快 |
常温下,相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中铝片先溶解完 |
| C |
结构和组成相似的物质,沸点随相对分子质量增大而升高 |
NH3沸点低于PH3 |
| D |
溶解度小的沉淀易向溶解度更小的沉淀转化 |
ZnS沉淀中滴加CuSO4溶液可以得到CuS沉淀 |
下列有关试剂的保存方法,错误的是( )
| A.浓硝酸保存在无色的玻璃试剂瓶中 |
| B.少量的钠保存在煤油中 |
| C.氢氧化钠溶液保存于带橡皮塞的玻璃试剂瓶中 |
| D.新制的氯水通常保存在棕色的玻璃试剂瓶中 |
新教材中编有较多的“资料”“阅读”“选学”内容,根据有关内容判断下列说法不正确的是( )
| A.玻尔用王水保存了诺贝尔奖章 |
| B.门捷列夫编制的第一张元素周期表,是按照相对原子质量排列的 |
| C.人体血液的pH>7 |
| D.BaCO3俗称“钡餐” |
下列各组中的物质,互为同位素的是( )
| A.白磷与红磷 | B.苯与甲苯 |
| C.重氢与超重氢 | D.2-甲基丙烷与丁烷 |
下列表示式正确的是( )
A.氨分子的电子式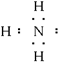 |
B.氢氧根离子的电子式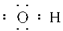 |
| C.乙酸的结构简式 C2H4O2 |
| D.苯的实验式 C6H6 |
在相同物质的量浓度的下列盐溶液中,c(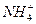 )最大的是()
)最大的是()
| A.NH4HSO4 | B.NH4HCO3 | C.CH3COONH | D.NH4Cl |