为了证明一水合氨(NH3·H2O)是弱电解质,甲、乙二人分别选用下列试剂进行实验:氨水、0.10 mol•L-1NH4Cl溶液、NH4Cl晶体、酚酞试液、pH试纸、蒸馏水。
(1)甲用pH试纸测出0.010mol•L-1氨水的pH为10,据此他认定一水合氨是弱电解质,你认为这一方法是否正确?___________ (填“正确”或“不正确”),并说明理由_______________________;
(2)乙取出10mL 0.010mol•L-1氨水,用pH试纸测其pH为a,然后用蒸馏水稀释至1000mL,再用pH试纸测其pH为b,若要确认NH3·H2O是弱电解质他认为只要a、b满足什么关系?________________;
(3)某温度下,pH均为4的盐酸和醋酸溶液分别加水稀释,其pH随溶液体积变化的曲线图中abc三点对应的溶液中水的电离程度由大到小的顺序是 ___________;该醋酸溶液稀释过程中,下列各量一定变小的是____________。
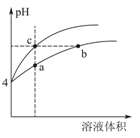
a.c(H+) b.c(OH-) c.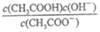 d.
d.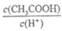
(4)在t℃时,某NaOH稀溶液中c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,则:①该温度下水的离子积常数Kw=___________(mol/L)-2;
②在该温度下,将100mL0.1mol/L的稀硫酸与100mL0.4mol/L的NaOH溶液混合后,溶液的pH=_________。
(1)化学键的键能是指气态原子间形成1 mol化学键时释放的能量。下表列出了某些化学键的键能:
| 化学键 |
H—H |
O==O |
O—H |
| 键能(kJ·mol-1) |
436 |
x |
463 |
请回答下列问题:
①如图表示某反应的能量变化关系图,此反应为 (填 “放热”或“吸热”)反应,其中ΔH= kJ·mol-1(用含C和D的字母表示)。
②若此能量变化关系图表示反应H2(g)+1/2O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1,则B= kJ·mol-1,x=
(2)①火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂。已知:
N2H4(l)+O2(g)=N2(g)+2H2O(g),ΔH=-534 kJ·mol-1
H2O2(l)=H2O(l)+ O2(g),ΔH=-98 kJ·mol-1
O2(g),ΔH=-98 kJ·mol-1
H2O(l)=H2O(g),ΔH=+44 kJ·mol-1
试写出N2H4和液态H2O2反应生成气态水的热化学方程式___________________。
②肼(N2H4)—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。该电池放电时,负极的电极反应式是_____________________。
标准状况下,22.4LHCl气体溶于50mL水再配成250mL溶液,求:
(1)所得盐酸的物质的量浓度为 ;
(2)若将此溶液再稀释成1L溶液,则稀释后盐酸的物质的量浓度变为 ;
(3)将(2)的溶液取出250mL与足量Zn反应可以产生的H2在标准状况下的体积为 。
用双线桥表示下列反应的电子转移方向和数目,并回答下列问题:
3I2 + 6NaOH = 5NaI + NaIO3 + 3H2O
(1) 是氧化剂, 是还原剂,氧化产物是 ;
(2)氧化剂与还原剂的物质的量之比为 ,当反应消耗3mol NaOH时,转移的电子数目为 。
相等质量的CO和CH4相比较,请完成下列问题。
(1)它们所含的分子数目之比为____________;
(2)同温同压时密度之比为___________;
(3)同温同体积时的压强之比为____________;
(4)同温同压时体积之比为___________。
(1)下列物质中,能导电的是 ,
(2)属于电解质的是 ,
(3)属于非电解质的是 。(填序号)
①饱和食盐水 ②液态HCl ③液态汞 ④固体BaSO4
⑤液态氨 ⑥熔融KNO3 ⑦干冰 ⑧蔗糖 ⑨干燥的空气