根据图回答问题.
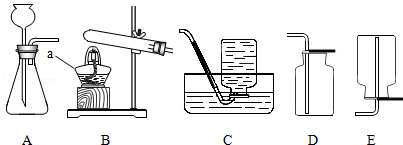
图中仪器a的名称是 .
用A与D相连可制取的一种气体是 ,该反应的化学方程式为 .
小明将B与C相连,用高锰酸钾制取氧气.实验操作有:a.停止加热b.固定试管c.将导管从水槽中取出d.装药品和放棉花e.加热,收集氧气.上述过程中缺少的一步操作是 ,将该操作编号为f,则正确的操作顺序是 .
查阅资料:相同条件下,氨气的密度比空气小,且易溶于水,其水溶液称为氨水;加热氯化铵和氢氧化钙固体混合物可制取氨气.根据所查资料,制取氨气应选择的装置是 .
下表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
| 温度/℃ |
0 |
20 |
40 |
60 |
80 |
100 |
|
| 溶解度/g |
Ca(OH)2 |
0.19 |
0.17 |
0.14 |
0.12 |
0.09 |
0.08 |
| NaOH |
31 |
91 |
111 |
129 |
313 |
336 |
|
(1)依据上表数据,绘制Ca(OH)2和NaOH的溶解度曲线,下图中能表示NaOH溶解度曲线的是 (填A或B)。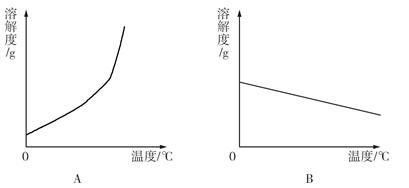
(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入氢氧化钙,②升高温度,③降低温度,④加入水,⑤蒸发水后再恢复到原温度,⑥加入生石灰。
其中措施正确的是 。
A.②④⑥B.③④C.①③⑤⑥D.①②⑤⑥
(3)20℃时,191g饱和NaOH溶液,蒸发10g水后,再降温到20℃,可析出NaOH晶体的质量为 。
(4)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后得到的溶液(乙溶液),此时溶液中溶质的质量分数乙 甲(填“>”、“<”或“=”)。
(5)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是 。
(6)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH (填“偏大”、“偏小”或“不受影响”)。
(1)用化学符号表示:
①3个二氧化碳分子 ;
②两个铜原子 ;
③碳酸钙中钙元素呈正二价 。
④地壳中含量最多的元素和金属元素形成的化合物 ;
⑤氯离子 ;
(2)水是生命之源,它与我们的生活密切相关。
①生活中,既能降低水的硬度,又能杀菌消毒的方法是 。
②电解水的装置如图所示,试管B中的气体是 ,通过此实验证明水是由 组成的,该反应的化学方程式是 。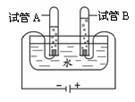
某化学兴趣小组为了测定当地的石灰石(主要成分是CaCO3)的质量分数,他们做了如下实验:取24克样品放入烧杯中,向其中逐渐加入100克一定质量分数的稀盐酸(杂质不溶于水也不与酸反应),所用盐酸的质量分数与剩余固体的质量关系如图所示,请根据图中的数据进行计算: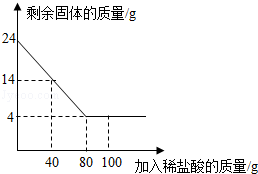
(1)石灰石样品中CaCO3的质量为 克.
(2)24克石灰石样品与盐酸充分反应后最多产生二氧化碳的质量为 克.
(3)求所用盐酸的溶质质量分数.(请根据化学方程式写出完整的计算步骤)
石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象:
| 次数 |
第1次 |
第2次 |
第3次 |
| 加入盐酸的质量/g |
10 |
10 |
10 |
| 剩余固体的质量/g |
16 |
12 |
8 |
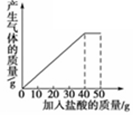
请计算:
(1)石灰石样品中杂质的质量为 g。
(2)所加盐酸的溶质质量分数.
“氯碱工业”是我国目前化学工业的重要支柱之一,它的主要原理是电解饱和食盐水,其化学方程式为xNaCl+2H2O xNaOH+H2↑+Cl2↑.在20℃时,取100g饱和NaCl溶液进行电解,一段时间后测得产生氯气(Cl2)的质量为7.1g.已知:20℃时,NaC1的溶解度为36g.
xNaOH+H2↑+Cl2↑.在20℃时,取100g饱和NaCl溶液进行电解,一段时间后测得产生氯气(Cl2)的质量为7.1g.已知:20℃时,NaC1的溶解度为36g.
请分析并计算回答:
(1)运用质量守恒定律可知上述反应中x= .
(2)通过计算,上述过程中同时产生H2的质量为 g.
(3)计算电解后剩余溶液中NaC1的质量分数(写出详细的计算过程,结果精确到0.1%).