下列关于氧化钠和过氧化钠的叙述正确的是
| A.Na2O2和Na2O都是白色固体,都能与冷水作用得到O2和NaOH |
| B.在Na2O2与水的反应中,氧化剂是Na2O2,还原剂是水 |
| C.相同物质的量的氧化钠和过氧化钠中阴离子物质的量之比为1:1 |
| D.Na2O与Na2O2都能与水反应生成碱,它们都是碱性氧化物 |
将铁和铝的混合粉末溶于过量盐酸中,通入足量氯气,再加入过量的NaOH溶液,最后溶液中大量存在的离子是
A.Na+、Fe2+、Cl-、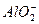 |
| B.Na+、Fe3+、Cl-、OH- |
C.Na+、Fe3+、Cl-、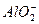 |
D.Na+、Cl-、OH-、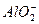 |
1993年8月,我国科学家利用超高真空扫描隧道显微镜在一块晶体硅的表面通过探针的作用搬走原子,写下了“中国”两字。下列说法不正确的是
| A.上述操作中发生了化学变化 |
| B.上述操作中只发生了物理变化 |
| C.这两个汉字是目前世界上最小的汉字 |
| D.这标志着我国科学已进入操作原子阶段 |
类推的思维方法在化学学习和研究中经常用到,但是有时会产生错误的结论。因此,推出的结论最终要经过检验才能决定其是否正确。以下几种类推结论不正确的是
| A.金属镁失火不能用CO2灭火器灭火;金属钠失火也不能用CO2灭火器灭火 |
| B.Fe3O4可以写成FeO·Fe2O3;Pb3O4也可以写成PbO·Pb2O3 |
| C.不能用电解AlCl3溶液来制取金属铝;也不能用电解MgCl2溶液来制取金属镁 |
| D.Al和S直接化合时可得到Al2S3;Fe与S直接化合时也可得到Fe2S3 |
下列说法正确的是
A.地壳中碳的含量居第一位
B.地壳中硅的含量居第二位
C.自然界中存在天然C单质,不存在天然Si单质
D.C、Si都能与强碱溶液反应,并放出H2
下列操作中加入(或通入)试剂至过量,最后无沉淀生成的是
| A.将CO2通入饱和Na2CO3溶液中 |
| B.将CO2通入Na2SiO3溶液中 |
| C.将SO2通入Ba(NO3)2溶液中 |
| D.将CO2通入漂白粉溶液中 |