下列实验操作正确的是( )
| A.稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中 |
| B.过滤操作时,为了加快过滤速率,可用玻璃棒不断搅拌过滤器中液体 |
| C.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D.将固体加入容量瓶中溶解并稀释至刻度,配制成一定物质的量浓度的溶液 |
下列关于胶体的叙述不正确的是
| A.用饱和FeCl3溶液滴入沸水中至红褐色,得到的Fe(OH)3胶体带正电荷 |
| B.胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9 ~ 10-7m之间 |
| C.用丁达尔效应可区别NaCl溶液和Fe(OH)3胶体 |
| D.Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的 |
下列物品所用材料为硅酸盐的是
| A.水晶镜片 | B.陶瓷餐具 | C.石英光导纤维 | D.计算机芯片 |
下列有关金属的叙述不正确的是
| A.目前我国流通的硬币是由合金材料制造的 |
| B.铁是人体必需的元素之一,主要以二价铁的形式存在血红蛋白中 |
| C.目前人类使用最广泛的金属材料是铝合金 |
| D.日用铝制品表面覆盖着氧化膜,对内部金属起保护作用 |
某温度时水的离子积常数为Kw。该温度下,将pH="a" 的一元酸HA与pH="b" 的一元碱BOH等体积混合,一定可以判定该溶液呈中性的依据是( )
| A.a + b ="Kw" |
| B.混合溶液的pH=7 |
C.混合溶液中,c(H+)= 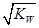 mol∙L−1 mol∙L−1 |
| D.混台溶液中,c(H+)+ c(B+) = c(OH-)+ c(A-) |
下列操作不能达到目的的是( )
| 选项 |
目的 |
操作 |
| A |
配制100 mL 1.0 mol/L CuSO4溶液 |
将25 g CuSO4·5H2O溶于100 mL蒸馏水中 |
| B |
除去KNO3中少量NaCl |
将混合物制成热的饱和溶液,冷却结晶,过滤 |
| C |
在溶液中将MnO4-完全转化为Mn2+ |
向酸性KMnO4溶液中滴加H2O2溶液至紫色消失 |
| D |
确定NaCl溶液中是否混有Na2CO3 |
取少量溶液滴加CaCl2溶液,观察是否出现白色浑浊 |