反应 4NH3(g)+5O2(g)  4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率v(X)(反应物的消耗速率或生成物的生成速率)可表示为
4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率v(X)(反应物的消耗速率或生成物的生成速率)可表示为
| A.v(NH3) ="0.010" mol/(L·s) | B.v(O2)="0.001" mol/(L·s) |
| C.v(NO) ="0.0010" mol/(L·s) | D.v(H2O) ="0.045" mol/(L·s) |
某有机化合物X,经过下列变化后可在一定条件下得到乙酸乙酯。则有机物X是()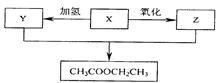
| A.C2H5OH | B.C2H4 | C.CH3CHO | D.CH3COOH |
现有三组混合液:①乙酸乙酯和碳酸钠溶液②乙醇和丁醇③溴化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是()
| A.分液、萃取、蒸馏 | B.萃取、蒸馏、分液 |
| C.分液、蒸馏、萃取 | D.蒸馏、萃取、分液 |
下列表示对应化学反应的离子方程式正确的是()
| A.向含有Fe2O3悬浊液中通入HI: Fe2O3 + 6H+= 2Fe3+ + 3H2O |
| B.将1 mol/L NaAlO2溶液和1.5 mol/L HCl溶液等体积互相均匀混合: 6AlO2-+9H++3H2O=5Al(OH)3↓+Al3+ |
| C.醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
| D.Ba(OH)2溶液中滴入NaHSO4溶液至完全Ba2+沉淀:2H++ SO42-+Ba2++2OH-=BaSO4↓+2H2O |
常温下,下列各组离子在溶液中能够大量共存,当溶液中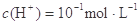 时,有气体产生:而当溶液中
时,有气体产生:而当溶液中 时,又能生成沉淀,则该组离子可能是()
时,又能生成沉淀,则该组离子可能是()
| A.Na+、Ba2+、NO3-、CO32- | B.Ba2+、K+、Cl—、NO3- |
| C.Mg2+、NH4+、SO42-、Cl- | D.Fe2+、Na+、SO42-、NO3— |
绿色化学的着眼点是使污染消灭在生产的源头,使整个合成过程和生产工艺对环境友好。其中合成方法应设计成能将所有的起始物质嵌入最终产物中,不产生任何废弃物,这时的原子利用率为100%。下列反应原子利用率可以达到100%的是()
| A.加成反应 | B.消去反应 |
| C.取代反应 | D.醇的催化氧化反应 |