图甲池和乙池中的四个电极都是惰性材料,请根据图示判断下列说法正确的是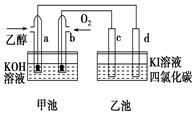
| A.两个装置之间没有盐桥,故不能形成电流 |
| B.a电极的电极反应式C2H5OH+16OH--12e-= 2CO+11H2O |
| C.一段时间后,乙池d电极周围的溶液呈现棕褐色 |
| D.乙池在反应前后溶液的pH不变 |
某溶液中,Fe3+、Cu2+、Fe2+的物质的量浓度之比为4:2:1,加入适量的铁粉,充分反应后,溶液中Fe3+、Cu2+、Fe2+的物质的量浓度之比变为1:1:2;则投入的铁粉与原溶液中Cu2+的物质的量之比为
| A.1:1 | B.1:2 | C.2:1 | D.2:3 |
下列有关物质的性质或结构的说法正确的是
A.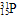 是一种广泛应用于含磷化合物的结构分析和医疗诊断的核素,其原子核内含有15个中子 是一种广泛应用于含磷化合物的结构分析和医疗诊断的核素,其原子核内含有15个中子 |
| B.Na的原子半径比Cl的大,但Na+的半径比Cl-的小 |
| C.Li、Na、K、Rb、Cs都属于碱金属元素,它们单质的还原性随原子序数的增大而减弱 |
| D.Cl与I同属于ⅦA族元素,则两者最高价氧化物对应水化物的酸性:HClO4<HIO4 |
下列叙述中正确的是:
| A.二氧化硅和干冰晶体熔化时所克服的作用力类型相同 |
| B.含有离子的晶体一定是离子晶体 |
| C.H2O是一种非常稳定的化合物,这是由于水分子中存在氢键 |
| D.分子晶体中不一定含有共价键,离子晶体中一定含有离子键 |
下列关于安全事故的处理方法中,正确的是
| A.金属钠着火时,立即用沾水的毛巾覆盖 |
| B.大量氯气泄漏时,迅速离开现场,并尽量往高处去 |
| C.不慎洒出的酒精在桌上着火时,立即用大量水扑灭 |
| D.少量浓硫酸沾在皮肤上,立即用大量氢氧化钠溶液冲洗 |
火法炼铜的原理为:Cu2S + O2="==" 2Cu + SO2,下列说法中,正确的是
| A.Cu2S 只做还原剂 | B.O2发生氧化反应 |
| C.S元素被氧化 | D.当0.8mol O2参加反应时,共转移了3.2mol电子 |