工业上将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2.在该反应中( )
| A.硫元素被氧化 |
| B.氧化剂与还原剂的物质的量之比为1:2 |
| C.每生成1molNa2S2O3,转移4mol电子 |
| D.相同条件下,每吸收10m3SO2就会放出2.5m3CO2 |
对危险化学品要在包装标签上印有警示性标志。在盛放NaOH固体的包装标签上应选用的标志是
根据下图海水综合利用的工业流程图,判断下列说法正确的是( )
已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
| A.过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质 |
| B.在过程③中将MgCl2·6H2O灼烧即可制得无水MgCl2 |
| C.在过程④、⑥反应中每氧化0.2 mol Br- 需消耗2. 24 L Cl2 |
| D.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题 |
下列有关同分异构体数目的叙述中,不正确的是( )
| A.甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种 |
| B.分子式符合C5H11Cl的化合物有6种 |
| C.已知二氯苯有3种同分异构体,则四氯苯的同分异构体的数目为3种 |
D.菲的结构简式为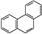 ,它与硝酸反应,可生成5种一硝基取代物 ,它与硝酸反应,可生成5种一硝基取代物 |
1.6mol CH4与Cl2发生取代反应,待反应完成后测得4种氯代物的物质的量依次增大0.2mol,则参加反应的Cl2为()
| A.5mol | B.2mol | C.2.5mol | D.4mol |
用NA表示阿伏加德罗常数,下列说法中,正确的是()
| A.常温常压下,3.0 g乙烷中含有的碳氢键数为0.7 NA |
| B.标准状况下,22.4 L C2H5OH中含有的氢原子数为6 NA |
| C.常温常压下,92 g的 NO2和N2O4混合气体含有的原子数为 6 NA |
| D.标准状况下,由Na2O2制得11.2 L O2,反应转移的电子数为0.5 NA |