下列有关性质的比较,不能用元素周期律解释的是( )
| A.热稳定性:Na2CO3>NaHCO3 | B.非金属性:Cl>Br\ |
| C.碱性:NaOH>Mg(OH)2 | D.酸性:H2SO4>H3PO4 |
对羟基扁桃酸是合成香料的重要中间体,它可由如下反应制得: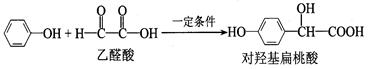
下列说法中,不正确的是
| A.上述反应的原子利用率是100% |
| B.对羟基扁桃酸的核磁共振氢谱有6个吸收峰 |
| C.对羟基扁桃酸可以发生加成反应、取代反应、消去反应和缩聚反应 |
| D.1 mol对羟基扁桃酸与足量NaOH溶液反应,消耗3 mol NaOH |
下列实验操作正确且能达到预期目的的是
| 选项 |
实验目的 |
操作 |
| A |
比较水和乙醇中羟基氢的活泼性强弱 |
用金属钠分别与水和乙醇反应 |
| B |
证明CH2=CHCHO中含有碳碳双键 |
滴入KMnO4酸性溶液 |
| C |
检验CH3CH2Br在NaOH溶液中是否发生了水解 |
将CH3CH2Br与NaOH溶液共热。冷却后,取出上层水溶液,用稀HNO3酸化,加入AgNO3溶液,观察是否产生淡黄色沉淀 |
| D |
除去苯中混有的苯酚 |
向混合液中加入过量浓溴水,充分反应后,过滤 |
尿黑酸是由酪氨酸在人体内非正常代谢而产生的一种物质。其转化过程如下: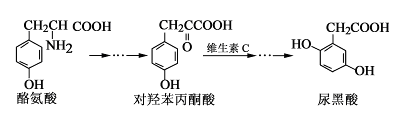
下列说法错误的是
| A.酪氨酸既能与盐酸反应,又能与氢氧化钠反应 |
| B.1 mol尿黑酸与足量浓溴水反应,最多消耗3molBr2 |
| C.对羟基苯丙酮酸分子中在同一平面上的碳原子至少有7个 |
| D.1 mol尿黑酸与足量NaHCO3反应,最多消耗3 molNaHCO3 |
下列有机物中,既能发生水解反应,又能发生银镜反应的是
| A.葡萄糖 | B.麦芽糖 | C.蔗糖 | D.甲酸甲酯 |
金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如下图。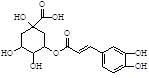
下列有关绿原酸的说法中不正确的是
| A.绿原酸分子中有4个手性碳原子 |
| B.绿原酸能发生显色反应、取代反应和加成反应 |
| C.每摩尔绿原酸最多与4 mol NaOH反应 |
| D.绿原酸分子中所有碳原子都能在同一平面上 |