25℃时,将V1 L PH="a" 的NaOH溶液和V2 L PH="b" 的盐酸溶液混合后,溶液呈中性。若a+b>14,则V1/V2的值为
| A.10a+b—14 | B.1014—a—b | C.1014+a—b | D.10a+b+14 |
下列各组中的离子,能在溶液中大量共存的是
| A.Mg2+、H+、C1-、OH- | B.Na+、Ba2+、CO 、NO 、NO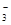 |
C.Na+、H+、Cl-、CO |
D.K+、Cu2+、NO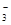 、SO 、SO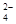 、 、 |
下列各组离子反应可用H++OH-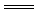 H2O表示的是
H2O表示的是
| A.氢氧化钡和硫酸 | B.氢氧化铁和盐酸 |
| C.醋酸和氢氧化钠 | D.硫酸氢钠和氢氧化钠 |
相同体积的NaCl溶液(浓度为C1)和Na2SO4溶液(浓度为C2),若其中的Na+ 物质的量浓度相同,则它们的物质的量浓度C1和C2的关系是
| A.C1>C2 | B.C1=C2 | C.C1<C2 | D.2 C1=C2 |
只用下列试剂中的一种就能鉴别Ba(NO3)2、Na2CO3、K2SO4三种溶液,则该试剂是
| A.KNO3溶液 | B.NaOH溶液 |
| C.稀H2SO4 | D.Na2SO4溶液 |
现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是
| A.分液、蒸馏、萃取 | B.萃取、蒸馏、分液 |
| C.分液、萃取、蒸馏 | D.蒸馏、萃取、分液 |