在标准状况下,将过量的铜粉投入到100ml 某稀HNO3中,用排水法收集到1.12 L气体,则该稀硝酸的物质的量浓度为?(写出计算过程)
实验室加热氯酸钾(KClO3)和二氧化锰(作催化剂)的混合物制取氧气(同时生成KCl)。若收集到标准状况下3.36L氧气,至少需要多少克氯酸钾?同时生成氯化钾的物质的量为多少?
把200 g 9.8%的稀硫酸与足量锌粒反应,求(1)能生成氢气多少克。(2)这些气体中所含分子个数为多少?(3)若欲用500mL集气瓶来收集这些氢气,则需准备几个集气瓶(设实验在标准状况下进行)?
取含MnO2的软锰矿石27.86g,跟足量浓盐酸反应,制得5.6L氯气(该状态下Cl2密度为3.17g/L)计算:
(1)这种软锰矿石中MnO2的质量分数?
(2)被氧化的HCl为多少g?
实验室用二氧化锰和浓盐酸反应制取氯气。
(1)若用200mL 10mol·L-1的浓盐酸与足量的二氧化锰固体加热反应(不考虑氯化挥发),则产生氯气的物质的量为0.50mol(填“大于”、“等于”或“小于”),原因是。
(2)8.7g二氧化锰与足量的浓盐酸反应,则被氧化的氯化氢的物质的量是多少?产生的氯气在标准状况下的体积是多少?
现将足量的浓硝酸与铜反应,生成4.48L的 气体(标况下),求:
气体(标况下),求:
(1)参加反应的铜的质量;
(2)被还原的硝酸的物质的量;
(3)将得到的溶液稀释到500ml,求溶液中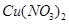 的物质的量浓度。
的物质的量浓度。