下列各表述与示意图不一致的是

(1)图①表示向含Mg2+、Al3+、NH4+的盐溶液中滴加NaOH溶液时,沉淀的物质的量和NaOH的体积的关系图。则三种离子的物质的量之比为______________________;
图②中曲线表示某反应过程的能量变化,当物质A(g)与B(g)反应生成物质C时,△H____0,若使用正催化剂,E值会_____________(增大、减小、不变)。
(2)在Cu2O/ZnO做催化剂的条件下,将CO(g)和H2O(g)充入容积为2L的密闭容器中合成CH3OH(g) ,反应过程中,CH3OH的物质的量(n)与时间(t)及温度的关系如图.根据题意回答下列问题:
①反应达到平衡时,平衡常数表达式K=______________;升高温度,K值____________(填“增大”、“减小”或“不变”).
②在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)= ____________;
③若其它条件不变,对处于Z点的体系,将体积压缩至原来的 1/2,达到新的平衡后,下列有关该体系的说法正确的是_________;
a.氢气的浓度与原平衡比减少 b.正、逆反应速率都加快
c.甲醇的物质的量增加 d.重新平衡时n(H2) /n(CH3OH)增大
④据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量的CO2有利于维持Cu2O的量不变,原因是_________________;(写出相关的化学方程式并辅以必要的文字说明).
烯烃通过臭氧氧化并经锌和水处理得到醛或酮,例如: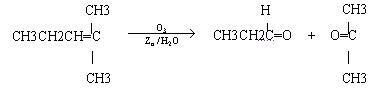
一种链状单烯烃A通过臭氧氧化并经锌和水处理得到B和C。化合物B含碳69.8%,含氢11.6%,B无银镜反应。D在浓硫酸存在下加热,可得到能使溴水褪色且只有一种结构的物质E。G的分子式为C7H14O2。有关转化关系如下;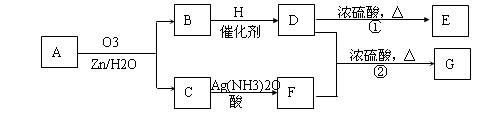
(1)B的相对分子质量是__________________。
(2)写出结构简式:A__________________、E_______________________。
(3)写出反应①、②的反应类型:①________________、②_______________。
(4)写出反应②的化学方程式:__________________________________________。
(5)F的一种同分异构体能发生酯化反应和银镜反应,其结构简式为__________。
下列是有机化合物A的转化过程: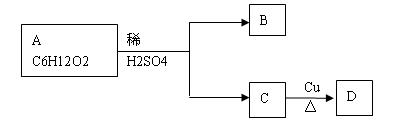
(1)若D在一定条件可以氧化为B,则A的结构简式:_______________________ 。
(2)若有 X、Y两物质与A是同类物质的同分异构体,也能发生上述转化。
①若B能发生银镜反应;C不能发生消去反应,则X的结构简式___________;
②若B,D均不能发生银镜反应;则Y的可能的结构简式_______________。
(3)若 Z与A为不同类别同分异构体,并且具有下列性质:
①Z不能与NaHCO3溶液反应;②Z不能使溴水褪色;
③1摩尔Z与足量金属钠反应可以生成1摩尔H2;
④Z分子的一氯取代产物只有二种(不考虑立体异构现象)。
则Z的结构简式_____________________ 。
超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式:2NO+2CO 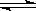 2CO2+N2;为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2;为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
| 时间/s |
0 |
1 |
2 |
3 |
4 |
5 |
| c(NO)/mol·L-1 |
1.00×10-3 |
4.50×10-4 |
2.50×10-4 |
1.50×10-4 |
1.00×10-4 |
1.00×10-4 |
| c(CO)/ mol·L-1 |
3.60×10-3 |
3.05×10-3 |
2.85×10-3 |
2.75×10-3 |
2.70×10-3 |
2.70×10-3 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应是________ 反应(填写“吸热”、“放热”)。
(2)前2s内的平均反应速度v(N2)=________。
(3)此反应的平衡常数表达式为K=________。
(4)假设在容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是________。
A .选用更有效的催化剂 B.升高反应体系的温度
.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
某反应体系中有物质:Bi2(SO4)3、NaMnO4、H2O、MnSO4、NaBiO3、Na2SO4、H2SO4。
(1)请将NaBiO3之外的反应物与生成物分别填入以下空格内。
(2)反应中,被氧化的元素是____________,氧化剂是___________。
(3)将氧化剂与还原剂及其已配平的化学计量数填入 下列空格中,并标出电子转移的方向和数目。
下列空格中,并标出电子转移的方向和数目。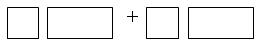
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E是人体内含量最高的金属元素。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的非金属性由强到弱的顺序为。
(2)B的氢化物的分子空间构型是______________ 。它是__________(填极性和非极性)分子。
(3)写出化合物AC2的电子式________;一种由B、C组成的化合物与AC2电子数相等,其化学式为_________________ 。
(4)E的核外电子排布式是________________。
(5)10molB的最高价氧化物对应的水化物的稀溶液与4molD的单质反应时,B被还原到最低价,B被还原后的产物化学式为____________。