下列关于溶液的说法错误的有几个
①NaHCO3溶液加水稀释,c(Na+)/c(HCO3-)的比值保持增大
②浓度均为0.1 mol/L的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO32-)+c(HCO3-)]
③在0.1 mol/L氨水中滴加0.l mol/L盐酸,恰好完全中和时溶液的pH=a,则由水电离产生的c(OH-)=l0-a mol/L
④向0.1mol/LNa2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO32-)均增大
⑤在Na2S稀溶液中,c(H+)=c(OH-)+c(H2S)+c(HS-)
| A.2个 | B.3个 | C.4个 | D.5个 |
下列叙述正确的是()
| A.168O2和188O2互为同位素,性质相似 |
| B.常温下,pH=1的水溶液中Na+、NO3-、HCO3-、Fe2+可以大量共存 |
| C.明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 |
| D.C(石墨, s) =C(金刚石, s);ΔH>0,所以石墨比金刚石稳定 |
已知Ba(AlO2)2可溶于水。下图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系。下列有关叙述正确的是()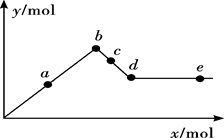
| A.a~b时沉淀的物质的量:Al(OH)3比BaSO4多 |
| B.c~d时溶液中离子的物质的量:AlO2-比Ba2+多 |
| C.a~d时沉淀的物质的量: BaSO4可能小于Al(OH)3 |
| D.d~e时溶液中离子的物质的量:Ba2+可能等于OH- |
上世纪50年代日本西部的婴儿大批发生贫血、腹泻、呕吐等症状,经调查都是食用“森永”牌奶粉所致,化验发现奶粉中含As量极高,As的来源是由于加入奶粉中的稳定剂Na2HPO4中含As严重超标。所以,切勿忽视添加剂的规格及级别,决不能随便代用。As在元素周期表中的位置是
| A.第四周期IVA族 | B.第五周期IVA族 |
| C.第四周期VA族 | D.第五周期VA族 |
设NA表示阿伏加德罗常数,下列说法不正确的是
| A.任何气体单质在标况下体积为22.4L时,则含有2NA个原子 |
| B.NA个C2H2分子中含有非极性共价键的数目为 NA个 |
| C.23克钠与足量氧气充分反应,转移的电子数为NA个 |
| D.在1L 1mol/L Na2S溶液中,含有NA个S2- |
如右图所示,一定条件下将1mol A2气体和3molB2气体充入一容积可变的密闭容器中,可滑动的活塞的位置如图1所示。在恒温恒压下发生如下反应:A2+3B22AB3。当反应达到平衡时,活塞位置如图2所示,则平衡时A的转化率是

| A.20% | B.40% | C.60% | D.无法确定 |