水的电离平衡曲线如图所示,下列说法不正确的是 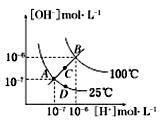
| A.图中四点KW间的关系:A=D<C<B |
| B.若从A点到C点,可采用温度不变在水中加少量的CH3COONa固体 |
| C.若从A点到D点,可采用温度不变在水中加入少量酸 |
| D.若处在B点所在的温度,将pH=2的硫酸与pH=10的NaOH的两种溶液等体积混合后,溶液显中性 |
“化学,我们的生活,我们的未来”曾经是2011年“国际化学年”的主题。你认为下列行为中,不符合这一主题的是
| A.控制含磷洗涤剂的生产和使用,防止水体富营养化,保护水资源 |
| B.研究采煤、采油新技术,尽量提高产量以满足工业生产的快速发展 |
| C.开发太阳能、水能、风能等新能源、减少使用煤、石油等化石燃料 |
| D.实现资源的“3R”利用,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、提高资源的循环利用(Recycle) |
足量铜粉与一定量的浓硝酸充分反应,得到硝酸铜溶液和 NO2、N2O4、NO 的混合气体,将这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体恰好完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol/L NaOH溶液至Cu2+恰好沉淀完全,则消耗 NaOH溶液的体积是()
| A.60 mL | B.45 mL | C.30 mL | D.15 mL |
向含1 mol HCl和l mol MgSO4的混合溶液中加入1 mol/L的Ba(OH)2溶液,产生沉淀的物质的量(n)与加入Ba(OH)2溶液体积(V)间的关系图正确的是()
将9.0 g铜和铁的混合物投入100mL稀硝酸中,充分反应后得到标准状况下1.12L NO,剩余4.8 g金属;继续加入100mL等浓度的稀硝酸,金属完全溶解,又得到标准状况下1.12L NO。若向反应后的溶液中加入KSCN溶液,溶液不变红,则下列说法正确的是()
| A.原混合物中铜和铁各0.075mol |
| B.稀硝酸的物质的量浓度为0.5mol·L-1 |
| C.第一次剩余4.8g金属为铜和铁 |
| D.再加入上述100mL稀硝酸,又得到标准状况下1.12L NO |
下图表示从固体混合物中分离X的两种方案,请根据方案1和方案2指出下列说法中合理的是()
| A.可以选用方案1分离碳酸氢钠的中含有的氯化铵 |
| B.方案1中残留物应该具有受热易挥发的性质 |
| C.方案2中加入的试剂一定能够与除X外的其它物质发生化学反应 |
| D.方案2中加入NaOH溶液可以分离出SiO2和Fe2O3混合物中的Fe2O3 |