已知反应:2CH3COCH3(l)⇌CH3COCH2COH(CH3)2(l).取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y﹣t)如图所示.下列说法正确的是( )

| A.b代表0℃下CH3COCH3的Y﹣t曲线 |
B.反应进行到20min末,CH3COCH3的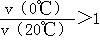 |
| C.升高温度可缩短反应达平衡的时间并能提高平衡转化率 |
D.从Y=0到Y=0.113,CH3COCH2COH(CH3)2的 |
下列有关物质的性质及应用说法正确的是()
| A.石英坩埚耐高温,可用来加热熔融氢氧化钠固体 |
| B.聚氯乙烯塑料在日常生活中可用来进行食品包装 |
| C.硫酸亚铁溶液和水玻璃在空气中久置后均变质 |
| D.甲醛可用作食品防腐剂 |
用NA表示阿伏加德罗常数的值,下列说法正确的是()
| A.22.4L氢气中含有的氢分子数目为NA |
| B.0.5molNa2CO3中含有的Na+数目为0.5NA |
| C.常温常压下,14g氦气含有的原子数目为NA |
| D.0.5moll/LFe2(SO4)3溶液中,SO42-的数目为1.5NA |
现代生活中出现了“铁强化酱油”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等商品,这里的铁、钙、硒、氟应理解为()
| A.元素 | B.单质 | C.分子 | D.氧化物 |
下列关于糖类、蛋白质、油脂的说法中,正确的是()
A.它们的组成元素中都有C、H、O、N等元素
B.在一定条件下,它们都能发生水解反应
C.人体需要的二十多种氨基酸都可以通过人体自身合成
D.油脂分为油和脂肪,它们都是高级脂肪酸的甘油酯
在含有大量的Fe3+、Cl-、SO42-的溶液中还可能大量存在的离子是()
| A.Ag+ | B.H+ | C.OH- | D.Ba2+ |