在25℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液,观察到的现象是先出现黄色沉淀,最终出现黑色沉淀。已知有关物质的溶度积KSP(25℃)如下:
| |
AgCl |
Agl |
Ag2S |
| KSP(单位省略) |
1.8×10-10 |
1.5×10-16 |
1.8×10-50 |
下列论述错误的是( )
A.沉淀转化的实质就是沉淀溶解平衡的移动
B.溶解度小的沉淀可以转化为溶解度更小的沉淀
C.AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶解度相同
D.25℃时,在饱和AgCl、AgI、Ag2S溶液中,所含Ag+的浓度不相同
根据表信息,判断以下叙述正确的是部分短周期元素的原子半径及主要化合价
| A.氢化物的稳定性为H2T<H2R | B.单质与稀盐酸反应的速率为L<Q |
| C.L2+与R2-的核外电子数相等 | D.M与T形成的化合物具有两性 |
下表给出几种氯化物的熔沸点,对此有下列说法: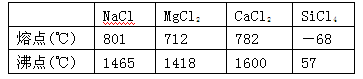
①CaCl2属于离子晶体 ②SiCl4是分子晶体③1500 ℃时,NaCl可形成气态分子④MgCl2水溶液不能导电。与表中数据一致的说法有
| A.仅① | B.仅④ | C.①和② | D.①②③ |
下列对一些实验事实的理论解释正确的是
| 选项 |
实验事实 |
理论解释 |
| A. |
NH3溶于水形成的溶液微弱导电 |
NH3是弱电解质 |
| B. |
氮气与氧气反应条件苛刻 |
氮元素的非金属性不强 |
| C. |
1体积水可以溶解700体积氨气 |
氢键的影响 |
| D. |
HF的沸点高于HCl |
H—F的键能比H—Cl的键能强 |
下列分子中的所有原子满足最外层8个电子结构结构的是
| A.HCl | B.BF3 | C.NCl3 | D.PCl5 |
现有如下各说法:①原子种类由原子核内质子数决定 ②全部由非金属元素形成的化合物一定为共价化合物③离子键是阳离子、阴离子之间的相互吸引 ④白磷晶体中,P4之间存在共价键 ⑤同素异形体在一定条件下的转化为物理变化。上述各种说法正确的是
| A.①②⑤正确 | B.都不正确 | C.④正确,其他不正确 | D.仅①不正确 |