把一块镁铝合金投入到1mol/L盐酸中,待合金完全溶解后,再往溶液里加入1mol/LNaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积的变化如图所示。下列说法中错误的是( )

| A.盐酸的体积为80mL | B.a的取值范围为0<a<50 |
| C.n(Mg2+)<0.025mol | D.当a值为30时,b值为0.01 |
N2O5是一种新型硝化剂,在一定温度下可发生下列反应:2N2O5(g)  4NO2(g)+O2(g) ΔH > 0T1温度下的部分实验数据为:
4NO2(g)+O2(g) ΔH > 0T1温度下的部分实验数据为:
| t/s |
0 |
500 |
1000 |
1500 |
| c(N2O5)/mol·L-1 |
5.00 |
3.52 |
2.50 |
2.50 |
下列说法不正确的是()
A.500 s内N2O5分解速率为2.96×10-3 mol·(L·s)-1
B.T1温度下的平衡常数为K1=125, 1000 s时转化率为50%
C.其他条件不变时,T2温度下反应到1000 s时测得N2O5(g)浓度为2.98 mol·L-1,则T1<T2
D.T1温度下的平衡常数为K1,T3温度下的平衡常数为K3,若K1>K3,则T1>T3
已知aA+、bB2+、cC-、dD2-四种离子均具有相同的电子层结构,关于A、B、C、D四种元素的叙述正确的是()
A. 原子半径:A>B>C>D B. 原子序数:b>a>c>d
C. 离子半径:D>C>B>A D. 失电子能力:B>A,得电子能力:D>C
如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若w原子最外层电子数是其内层电子数的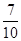 ,则下列说法中不正确的是()
,则下列说法中不正确的是()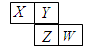
| A.最高价氧化物对应水化物的酸性:W > Z |
| B.Y元素的两种同素异形体在常温下都是气体 |
| C.原子半径由大到小排列顺序:Z >Y >X |
| D.气态氢化物的稳定性:Y > X |
元素周期表里金属元素和非金属元素分界线附近能找到()
| A.制农药元素 | B.制催化剂元素 |
| C.制半导体元素 | D.制耐高温合金元素 |
两份铝屑,一份与过量HCl反应,另一份与过量NaOH溶液反应,产生的H2体积比为1:2,则两份铝屑的质量比为()
| A.1:2 | B.1:1 | C.1:3 | D.2:1 |