一定温度下,可逆反应2NO2(g)  2NO(g)+O2(g)在体积固定的密闭容器中反应,达到平衡状态的标志是
2NO(g)+O2(g)在体积固定的密闭容器中反应,达到平衡状态的标志是
①单位时间内生成n mol O2,同时生成2n mol NO2
②单位时间内生成n mol O2,同时生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2∶2∶1
④混合气体的压强不再改变
⑤混合气体的颜色不再改变
⑥混合气体的平均相对分子质量不再改变
| A.①④⑤⑥ | B.①②③⑤ | C.②③④⑥ | D.以上全部 |
分子式为C10H20O2的有机物A,能在酸性条件下水解生成有机物C和D,且C在一定条件下可转化成D,则A的可能结构有()
| A.2种 | B.3种 | C.4种 | D.5种 |
在105℃时1L两种气态混合烃与9L氧气混合,充分燃烧后恢复到原状态,所得气体体积为10.5L,再将气体通过碱石灰,体积缩小6L。则下列各组混合烃中符合此条件的是()
| A.CH4,C4H8 | B.CH4,C4H10 | C.C2H4,C3H8 | D.C2H2,C4H10 |
下列化合物中,既能发生消去反应生成烯烃,又能发生水解反应的是()
某单烯烃与H2加成后的产物是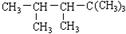 ,则该烯烃的结构式可能有()
,则该烯烃的结构式可能有()
| A.1种 | B.2种 | C.3种 | D.4 种 |
以2—氯丙烷为主要原料制1,2—丙二醇CH3CH(OH)CH2OH时,经过的反应为()
| A.加成—消去—取代 | B.消去—加成—取代 |
| C.取代—消去—加成 | D.取代—加成—消去 |