常温下,下列溶液中的微粒浓度关系正确的是
| A.新制氯水中加入固体NaOH: c(Na+)=c(Cl-)+c(ClO-)+c(OH-) |
| B.pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3—)>c(CO32—)>c(H2CO3) |
| C.pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH+4)>c(OH-)=c(H+) |
| D.0.2mol·L-1CH3COOH溶液与0.1 mol·L-1 NaOH溶液等体积混合:2c(H+)-2c(OH-)=c(CH3COO-)-c (CH3COOH) |
下列各组物质中属于同分异构体的是
| A.正丁烷和异丁烷 | B.金刚石和石墨 | C.12 C和13C | D.乙烯和乙烷 |
下列各项中表达正确的是()
A.F原子结构示意图: |
B.H2O的电子式: |
| C.1H、2H、3H是三种不同元素 | D.乙烯的分子式: C2H4 |
环境污染已成为人类社会面临的重大威胁,各种污染数不胜数。下列名词与环境污染无关的是
①温室效应 ②赤潮 ③酸雨 ④光化学污染 ⑤臭氧层空洞 ⑥水俣病 ⑦潮汐 ⑧大脖子病
| A.①②③ | B.⑦⑧ | C.①⑤⑥ | D.②⑤⑦ |
下列物质不属于天然高分子化合物的是
| A.淀粉 | B.蚕丝 | C.葡萄糖 | D.纤维素 |
A、B、C、D、E都是中学化学中常见物质,它们均含有同一种短周期元素,在一定条件下可发生如图所示的转化,其中A是单质,B在常温下是气态氢化物,C、D是氧化物,E是D和水反应的产物。下列判断中不合理的是( )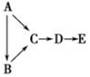
A.A不可能是金属B.由C生成D肯定发生了电子转移
C.由A生成C肯定属于离子反应D. B与E可能反应生成盐