SO2 、CO 、NOx 是对环境影响较大的气体,对它们的合理控制和治理是优化我们生存环境的有效途径。请回答下列问题:
(1)已知25℃、101kPa时:
2SO2(g) + O2(g)  2SO3(g) △H1 =" -" 197 kJ•mol-1
2SO3(g) △H1 =" -" 197 kJ•mol-1
H2O(g) = H2O(l) △H2 =" -" 44 kJ•mol-1
2SO2(g) + O2(g) + 2H2O(g) = 2H2SO4(l) △H3 =" -" 545 kJ•mol-1
则SO3(g)与H2O(l)反应的热化学方程式是 ;
(2)若反应2H2(g)+ O2 (g)═ 2H2O(g ),△H=-241.8kJ•mol-1。根据下表数据, 则x="______" kJ•mol-1;
| 化学键 |
H-H |
O═O |
O-H |
| 断开1mol化学键所需的能量/kJ |
436 |
x |
463 |
(3)甲醇汽油也是一种新能源清洁燃料。工业上可用CO和H2制取甲醇,热化学方程式为:CO(g)+2H2(g) CH3OH(g) △H="-90" kJ•mol-1。某温度下,在两个容积均为1 L的密闭容器中,分别发生该反应:
CH3OH(g) △H="-90" kJ•mol-1。某温度下,在两个容积均为1 L的密闭容器中,分别发生该反应:
| 容器 |
甲 |
乙 |
| 反应物投入量 |
1 mol CO (g)和2 mol H2(g) |
1 mol CH3OH(g) |
| 平衡时c(CH3OH) |
c1 |
c2 |
| 平衡时能量变化 |
放出54kJ |
吸收a kJ |
则 c1_________ c2(填“>”或“<”或“=”) , a=____________;
(4)氮氧化物都是常见的大气污染物,某温度下氮氧化物与悬浮在大气中的海盐粒子相互作用时,涉及如下反应:
i. 2NO(g)+Cl2(g) 2ClNO(g) △H1< 0 其平衡常数为K1
2ClNO(g) △H1< 0 其平衡常数为K1
ii. 2NO2(g)+NaCl(s)  NaNO3(s)+ClNO(g) △H2<0 其平衡常数为K2
NaNO3(s)+ClNO(g) △H2<0 其平衡常数为K2
①现有反应4NO2(g)+2NaCl(s)  2NaNO3(s)+2NO(g)+Cl2(g), 则此反应的平衡常数K3= (用K1、K2表示);
2NaNO3(s)+2NO(g)+Cl2(g), 则此反应的平衡常数K3= (用K1、K2表示);
②为研究不同条件对反应ii的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO2和足够的NaCl(s),10min时反应ii达到平衡。测得平衡时NO2的转化率α1(NO2) =50%,则10min内υ(ClNO) = ,平衡常数K2= ;若其它条件不变,使反应在恒压条件下进行,平衡时NO2转化率为α2(NO2),则:α1(NO2) α2(NO2)(填“>”“<”或“=”)。
③工业上利用氨还原法除去氮氧化合物,生成两种对环境友好的物质。请以氮氧化合物的通式NOX写出化学方程式: 。
已知乙烯能发生以下转化:
(1)乙烯的结构简式为:
(2)写出反应的化学方程式
①:反应类型:
②: 反应类型:
(共12分)已知乳酸的结构简式为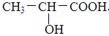 。试回答:
。试回答:
(1)乳酸分子中含有___________和___________两种官能团(填官能团名称)
(2)乳酸跟氢氧化钠溶液反应的化学方程式:____________________________________。
(3)乳酸跟足量的金属钠反应的化学方程式:_____________________________。
(4)乳酸跟乙醇发生酯化反应的化学方程式:____________________________,
(5)两个乳酸分子间发生酯化反应生成的环酯(C6H8O4)的结构简式为:__________。
医院里检验糖尿病的方法是将病人尿液加入到CuSO4和NaOH的混合液中,加热后产生砖红色沉淀,说明病人的尿中含有;检验淀粉是否完全水解的试剂。
(1)苯与甲烷都能发生反应,反应的主要差异表现在
(2)苯与乙烯都能发生反应,反应的差异主要表现在
(3)乙烯能使酸性高锰酸钾溶液褪色和溴的四氯化碳溶液褪色,其中与高锰酸钾发生的反应是反应(填反应类型,下同);与溴水发生的反应是反应。
为了检验和除去下表中的各种杂质(括号里的物质),请从(I)中选出适当的检验试剂,从(II)中选出适当的除杂试剂,将所选的答案的括号填入相应的空格内。
| 物质 |
检验试剂 |
除杂试剂 |
| 甲烷(乙烯) |
||
| 酒精(水) |
(I)检验的试剂:A. 无水硫酸铜 B.酸性高锰酸钾溶液 C.盐酸 D.氢氧化钠溶液
(II)除杂试剂:a.硫酸 b.酸性高锰酸钾溶液 c.新制的生石灰 d.溴水