短周期主族元素X、Y、Z、W的原子序数依次增大。X与W同主族,X、W的单质在标准状况下的状态不同。Y是空气中含量最高的元素,Z原子最外层电子数是其内层电子总数的3倍,Z2-与W+具有相同的电子层结构。下列说法正确的是
| A.原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X),离子半径大小顺序:r(Z2-)>r(W+) |
| B.元素Y的简单气态氢化物的热稳定性和熔沸点都比Z的高 |
| C.由X、Y、Z三种元素形成的化合物的水溶液可能呈碱性 |
| D.化合物X2Z2与W2Z2所含化学键类型完全相同 |
下列实验可达到实验目的的是
A.将 与NaOH的醇溶液共热制备CH3—CH==CH2 与NaOH的醇溶液共热制备CH3—CH==CH2 |
B.乙酰水杨酸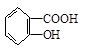 与适量NaOH溶液反应制备 与适量NaOH溶液反应制备 |
| C.向CH3CH2Br中滴入AgNO3溶液以检验溴元素 |
| D.甲苯在溴化铁催化作用下与液溴反应生成2,4,6-三溴甲苯 |
人体气味的成分中含有以下化合物:①辛酸;②壬酸;③环十二醇;④5,9一十一烷酸内酯;⑤十八烷⑥己醛;⑦庚醛。下列说法正确的是
| A.①、②、⑥分子中碳原子数小于10,③、④、⑤分子中碳原子数大于10 |
| B.①、②是无机物,③、⑤、⑦是有机物 |
| C.①、②是酸性化合物,③、⑤不是酸性化合物 |
| D.②、③、④含氧元素,⑤、⑥、⑦不含氧元素 |
某烃的分子式为C8H10,不能使溴水褪色,但可使酸性KMnO4溶液褪色,则此烃的结构有
| A.2种 | B.3种 | C.4种 | D.5种 |
下列物质中存在顺反异构体的是
| A.2-氯丙烯 | B.丙烯 | C.2-丁烯 | D.1-丁烯 |
下列名称的有机物实际上不可能存在的是
| A.3,3二甲基2戊烯 | B.2甲基4乙基1己烯 |
| C.3甲基2戊烯 | D.2,2二甲基丁烷 |