用NA表示阿伏加德罗常数的值。下列叙述中正确的是
| A.常温常压下1.6 g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA |
| B.1.0 L 1.0 mol·L-1的NaAlO2水溶液中含有的氧原子数为2NA |
| C.18 g D2O含有NA个质子 |
| D.0.5 mol·L-1硫酸钾溶液中阴离子所带电荷数为NA |
能证明某物质是弱电解质的是
| A.难溶于水 |
| B.溶液中存在已电离的离子和未电离的分子 |
| C.水溶液的导电性差 |
| D.熔融状态时不导电 |
下图为番茄电池,下列说法正确的是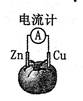
| A.一段时间后,锌片质量会变小 |
| B.铜电极附近会出现蓝色 |
| C.电子由铜通过导线流向锌 |
| D.锌电极是该电池的正极 |
被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰。在纸内的离子“流过”水和氧化锌组成的电解液。电池总反应为:Zn+2MnO2+H2O=ZnO+2MnO(OH)。下列说法正确的是
| A.该电池的正极为锌 |
| B.电池正极反应式为:MnO2 + e-+H2O =" MnO(OH)" + OH- |
| C.该电池反应中二氧化锰起催化剂作用 |
| D.当 0.l mol Zn 完全溶解时,流经电解液的电子数目为 1.204×l023 |
下列说法不正确的是
| A.0.1mol/L硫酸铵溶液中各离子的浓度由大到小的顺序是:c (NH4+)>c(SO42-)>c(H+)>c(OH-) |
| B.在苏打与小苏打的混合溶液中存在:c(Na+)+c(H+) ="c(OH" -)+2c(CO32-)+c(HCO3-) |
| C.在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去,证明Na2CO3溶液中存在水解平衡 |
| D.常温常压下能自发进行的反应,一定都是放热反应 |
下列说法中正确的是
| A.已知H+(aq)+OH-(aq) = H2O(l) ΔH=-57.3kJ/mol,则浓硫酸与稀NaOH溶液反应、稀醋酸与稀NaOH溶液反应所测得的中和热都为ΔH=-57.3kJ/mol |
| B.由C(石墨,s)= C(金刚石,s)ΔH=+1.9kJ/mol,可知金刚石比石墨稳定 |
| C.在用标准盐酸滴定未知浓度氢氧化钠溶液的实验中,若用待测液润洗锥形瓶,则测定结果偏低(其他操作正确) |
D.向存在着FeCl3 (黄色)+3KSCN  Fe(SCN) 3(血红色) +3KCl平衡体系的溶液中,加少量KCl固体,溶液血红色不发生变化 Fe(SCN) 3(血红色) +3KCl平衡体系的溶液中,加少量KCl固体,溶液血红色不发生变化 |