铅蓄电池的工作原理为Pb+PbO2+4H++2SO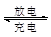 2PbSO4+2H2O。下图所示装置中,A为PbO2电极,B为Pb电极,E、F均为PbSO4电极,U形管中盛有足量硫酸溶液。先闭合S1足够长时间后断开S1,下列有关说法中不正确的是( )
2PbSO4+2H2O。下图所示装置中,A为PbO2电极,B为Pb电极,E、F均为PbSO4电极,U形管中盛有足量硫酸溶液。先闭合S1足够长时间后断开S1,下列有关说法中不正确的是( )
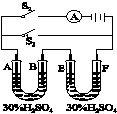
A.闭合S1时,左侧U形管为原电池,右侧U形管为电解池,F电极上生成氧气
B.若将两U形管中的溶液混合,混合液的质量分数仍为30%
C.若再单独闭合S2,电极A、B的质量会逐渐增加,电极E、F的质量会逐渐减小
D.若再单独闭合S2,E、F电极上发生的反应与之前相同
若甲烷与氯气以物质的量之比1:3混合,在光照下得到的产物:⑴CH3Cl,⑵CH2Cl2,⑶CHCl3,⑷CCl4,其中正确的是()
| A.只有⑴ | B.只有⑶ |
| C.⑴⑵⑶的混合物 | D.⑴⑵⑶⑷的混合物 |
|
A、B、C都是金属,A中混有C时,A先腐蚀;A与B组成原电池时,A为电池的正极,则A、B、C三种金属的活动性顺序为()
A.A>B>C B.A>C>B C.B>A>C D.B>C>A下列反应原理中,不符合工业冶炼金属实际情况的是()
A.2HgO 2Hg+O2↑ 2Hg+O2↑ |
B.2Al+3MnO2 2Al2O3+3Mn 2Al2O3+3Mn |
C.2MgO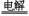 2Mg+O2↑ 2Mg+O2↑ |
D.4CO+Fe3O4 3Fe+4CO2 3Fe+4CO2 |
可逆反应达到化学平衡的标志是()
| A.正、逆反应不再进行 | B.反应物的浓度为零 |
| C.正、逆反应都还在继续进行 | D.正、逆反应的速率相等 |
某金属能和盐酸反应生成氢气,该金属与锌组成原电池时,锌为负极,则该金属可能为
()
| A.铝 | B.铜 | C.锡 | D.硅 |