室温时,关于下列溶液的叙述正确的是( )
| A.1.0×10-3 mol·L-1盐酸的pH=3,1.0×10-8 mol·L-1的盐酸pH=8 |
| B.pH=a的醋酸溶液稀释1倍后,溶液的pH=b,则a>b |
| C.pH=12的氨水和pH=2的盐酸等体积混合,混合液的pH<7 |
| D.1 mL pH=1的盐酸与100 mL NaOH溶液混合后溶液的pH=7,则NaOH溶液的pH=11 |
根据元素在周期表中的位置判断,下列元素中原子半径最小的是
| A.氧 | B.氟 | C.碳 | D.氮 |
用NA代表阿伏加德罗常数的值,下列有关说法正确的是
| A.3mol NO2与足量H2O反应,转移的电子数为NA |
| B.常温常压下,22.4L氦气含有NA个氦原子 |
| C.标准状况下,22.4L单质溴所含有的原子数目不为2NA |
| D.钠在氧气中燃烧,1 mol O2作氧化剂时得到的电子数为4NA |
下列反应的离子方程式书写正确的是
| A.用FeCl3溶液腐蚀印刷电路板:Fe3++Cu=Fe2++Cu2+ |
| B.氯气跟水反应:Cl2 + H2O= H+ + Cl- + HClO |
| C.钠与水的反应:Na+H2O=Na++OH-+H2↑ |
| D.AlCl3溶液中加入足量的氨水:Al3++ 3OH- ══ Al(OH)3↓ |
下列装置所示的实验中,能达到实验目的的是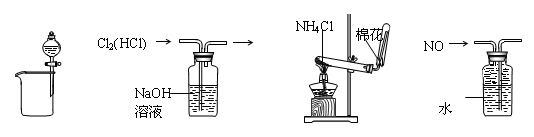
| A.分离碘和酒精 | B.除去Cl2中的HCl | C.实验室制氨气 | D.排水法收集NO |
少量的金属钠长期暴露在空气中,它的最终产物是
| A.NaOH | B.Na2CO3·10H2O |
| C.Na2CO3 | D.NaHCO3 |