人工光合作用能够借助太阳能,用CO2和H2O制备化学原料。科学家用氮化镓材料与铜组装如图的人工光合系统,成功地实现了以CO2和H2O合成CH4,下列说法不正确的是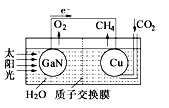
| A.该过程是将太阳能转化为化学能的过程 |
| B.GaN表面发生氧化反应,有O2产生 |
| C.电解液中的H+从质子交换膜右侧向左侧迁移 |
| D.Cu表面的电极反应式CO2+8e-+8H+=CH4+2H2O |
某有机物分子中含有强还原性基团,将其与苛性钠溶液共煮后,可得到两种有机物,其中一种仍有强还原性,则该有机物可能是
下列说法正确的是
①制乙酸乙酯时,把乙醇和乙酸依次加入浓硫酸中②用灼烧的方法可以区别丝和棉花
③油脂水解可得到氨基酸和甘油④纤维素和淀粉都是多糖,二者互为同分异构体
⑤溴乙烷、油脂和蛋白质在一定条件都能水解⑥乙醇中是否含水,可用金属钠来检验
⑦乙烯和乙烷都能发生加聚反应⑧蛋白质水解的最终产物是多肽
| A.①②③⑧ | B.②⑤ | C.④⑤⑥⑦ | D.①⑤ |
下列离子方程式正确的是
| A.实验室用大理石与醋酸反应制取二氧化碳:CaCO3+2H+=Ca2++CO2↑+H2O |
| B.氯乙酸与氢氧化钠溶液共热: CH2ClCOOH+OH-→CH2ClCOO-+H2O |
C.苯酚钠溶液中通入少量二氧化碳: 2C6H5O-+CO2+H2O→2C6H5OH+CO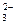 |
| D.用银氨溶液检验乙醛中的醛基: |
CH3CHO +2[Ag(NH3)2]+ + 2OH-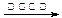 CH3COO-- + NH4+ +3NH3 + 2Ag↓+ H2O
CH3COO-- + NH4+ +3NH3 + 2Ag↓+ H2O
由一个氧原子,一个氮原子,7个氢原子和若干个碳原子组成的有机物,其碳原子的个数至少为
| A.2 | B.3 | C.4 | D.5 |
玻璃器皿上沾有一些用水洗不掉的残留物,其洗涤方法正确的是
①残留在试管内壁上的碘,用酒精洗涤②盛放过苯酚的试剂瓶中残留的苯酚,用酒精洗涤③做银镜反应后试管壁上银镜,用稀氨水洗涤④沾附在试管内壁上的油脂,用热碱液洗涤
| A.①③④ | B.①②④ | C.②③④ | D.①②③④ |