设NA为阿伏伽德罗常数的值。下列说法正确的是
A.5NH4NO3 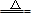 2HNO3+4N2↑+9H2O反应中,生成28 g N2,转移的电子数目为3.75NA 2HNO3+4N2↑+9H2O反应中,生成28 g N2,转移的电子数目为3.75NA |
| B.室温下,1 L pH=13的NaOH溶液中,由水电离的OH- 数目为0.1NA |
| C.氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2NA |
| D.高温下,0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3 NA |
丙烯与某气态烃组成的混合气完全燃烧时,所需氧气的体积是混合气体体积的5倍(相同状况),则该气态烃是( )
| A.C4H8 | B.C3H4 | C.C2H6 | D.C2H4 |
0.1mol化合物甲在足量的氧气中完全燃烧后生成4.48LCO2(标况下测量),推测甲是
| A.CH4 | B.C2H4 | C.C3H6 | D.C6H6 |
要对热稳定的高沸点液态有机物和低沸点的杂质的混合物进行提纯一般使用的方法是
| A.蒸馏 | B.重结晶 | C.过滤 | D.萃取 |
实验式相同,既不是同系物,又不是同分异构体的是( )
| A.1辛烯和3甲基1丁烯 | B.苯和乙炔 |
| C.1氯丙烷和2氯丙烷 | D.甲苯和乙苯 |
据报道1991-1996年人类发现和创制的化合物已有1000多万种,这正好相当于到1990年以前人类在1000多年来已知物质的总量;此外,关于物质的信息量也剧增。请你推断:新发现和新创制的物质主要是()
| A.放射性同位素 | B.无机物 | C.有机化合物 | D.烃类物质 |