高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
| A.放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2 |
B.充电时阳极反应为:Fe(OH)3-3e-+5OH-=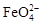 +4H2O +4H2O |
| C.放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化 |
| D.放电时正极附近溶液的碱性增强 |
最近意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如图所示,已知断裂1molN-N吸收193kJ热量,生成1molN≡N放出941kJ热量。根据以上信息和数据,下列说法正确的是 ( )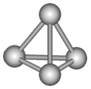
| A.N4属于一种新型的化合物 | B.N4是N2的同系物 |
| C.N4转变为N2是物理变化 | D.1molN4气体转变为N2放出724kJ能量 |
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g) = CO2(g)+3H2(g);DH=+ 49.0 kJ·mol-1
②CH3OH(g)+1/2O2(g) = CO2(g)+2H2(g);DH =-192.9 kJ·mol-1下列说法正确的是
| A.CH3OH的燃烧热为192.9 kJ·mol-1 |
| B.CH3OH的燃烧热为133.9 kJ·mol-1 |
| C.CH3OH转变成H2的过程一定要吸收能量 |
| D.根据②推知反应:CH3OH(l) +1/2O2(g) = CO2(g) +2H2(g)的DH >-192.9 kJ·mol-1 |
有一种不纯的铁,已知它含有铜、铝、钙或镁中的一种或几种,将5.6克样品跟足量稀H2SO4完全反应生成0.2克氢气,则此样品中一定含有( )
| A.Cu | B.Al | C.Ca | D.Mg |
科学家已发现一种新型氢分子,其化学式为H3,在相同条件下,等质量的H2和H3,具有相同的( )
| A.分子数 | B.原子数 | C.体积 | D.物质的量 |
常温常压下,某容器真空时质量为201.0 g,当它盛满甲烷(CH4)时质量为203.4 g,而盛满某气体Y时质量为205.5 g,则Y气体可能是( )
| A.O2 | B.NO | C.C2H6 | D.CO2 |