I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)=I3-(aq) , 某 I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是: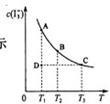
| A.反应I2(aq)+I-(aq)=I3-(aq)的△H>0 |
| B.若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1<K2 |
| C.若反应进行到状态D时,一定有v正>v逆 |
| D.状态A与状态B相比,状态A的c(I2)大 |
将氨水缓缓地滴入盐酸中至中性,下列有关的说法正确的是:①盐酸过量②氨水过量 ③恰好完全反应④c (NH4+) = c(Cl-)⑤c (NH4+) < c(Cl-)
| A.①⑤ | B.③④ | C.②⑤ | D.②④ |
下列水解的离子方程式正确的是
A.HS-+H2O S2-+H3O+ S2-+H3O+ |
B.Fe3++3H2O Fe(OH)3↓+3H+ Fe(OH)3↓+3H+ |
C.CO32-+2H2O H2CO3+2OH- H2CO3+2OH- |
D.NH4++H2O NH3·H2O+H+ NH3·H2O+H+ |
下列叙述的说法不正确的是
| A.金属的电化学腐蚀比化学腐蚀更普遍 |
| B.用牺牲锌块的方法来保护船身 |
| C.用铝质铆钉铆接铁板,铁板易被腐蚀 |
| D.在镀件上电镀锌,用锌作阳极 |
在标准状况下①6.72L CH4②3.01×1023个HCl分子③13.6g H2S ④0.2mol NH3,下列对这四种气体的关系从大到小表达错误的是
|
A.体积②>③>①>④ B.密度②>③>①>④
C.质量②>③>①>④ D.氢原子个数①>③>④>②某无色混合气体中可能含有O2、SO2、NO 、NO2、CO、CO2中的气体。现将此透明的混合气体通过品红溶液后,品红溶液褪色,再通入澄清石灰水,石灰水变浑浊。把剩余气体排入空气中,很快变为红棕色。对于原混合气体成分的判断中错误的是
| A.肯定有SO2、CO2和NO | B.肯定没有O2和NO2 |
| C.可能有CO和CO2 | D.肯定有SO2和NO |