下列相关实验不能达到预期目的的是
| |
相关实验 |
预期目的 |
| A |
向少量燃尽火柴头的浸泡液中滴加足量稀HNO3、AgNO3 |
验证火柴头含有氯元素 |
| B |
试样加水溶解后,再加入足量Ba(OH)2溶液,有白色沉淀生成 |
检验NaHCO3固体中是否含 Na2CO3 |
| C |
向溶液中加NaOH溶液后加热,产生使湿润的红色石蕊试纸变蓝的气体 |
证明原溶液中含有NH4+ |
| D |
两支试管中装有等体积、等浓度的H2O2溶液,向其中一支试管中加入FeCl3溶液 |
探究FeCl3溶液对H2O2分解速率的影响 |
目前人类已发现几千万种物质,对物质进行分类,有利于我们的学习。下列物质的分类不正确的是
| A.SO2(酸性氧化物) | B.氨水(弱电解质) | C.HNO3(含氧酸) | D.氯水(混合物) |
香兰素是重要的香料之一,它可由丁香酚经多步反应合成
有关上述两种化合物的说法正确的是
| A.常温下,1 mol丁香酚只能与1 mol Br2反应 |
| B.丁香酚不能与FeCl3溶液发生显色反应 |
| C.香兰素分子中至少有12个原子共平面 |
| D.1 mol香兰素最多能与3 mol氢气发生加成反应 |
北京残奥会吉祥物是以牛为形象设计的“福牛乐乐”。有一种有机物的键线式也酷似牛,如下图所示,故称为牛式二烯炔醇。下列有关说法不正确的是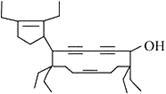
| A.牛式二烯炔醇含有3种官能团 |
| B.牛式二烯炔醇分子内能发生消去反应 |
| C.1 mol牛式二烯炔醇最多可与6 molBr2发生加成反应 |
| D.牛式二烯炔醇可发生取代反应 |
分枝酸可用于生化研究。其结构简式如图。下列关于分枝酸的叙述正确的是
| A.分子中含有2种官能团 |
| B.可与乙醇、乙酸反应,且反应类型相同 |
| C.1mol分枝酸最多可与3molNaOH发生中和反应 |
| D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同 |
常见的有机反应类型有①取代反应 ②加成反应 ③消去反应 ④酯化反应 ⑤加聚反应 ⑥缩聚反应 ⑦还原反应,其中在有机物中引入羟基的反应类型有
| A.①②④ | B.⑤⑥⑦ | C.①②⑦ | D.③④⑥ |