微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如下图所示。下列有关说法错误的是
| A.正极反应中有CO2生成 |
| B.微生物促进了反应中电子的转移 |
| C.质子通过交换膜从负极区移向正极区 |
| D.电池总反应为C6H12O6+6O2=6CO2+6H2O |
下列实验现象预测正确的是

| A.实验I:振荡后静置,上层溶液颜色保持不变 |
| B.实验II:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 |
| C.实验III:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 |
| D.实验IV:继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应 |
某有机物X的结构简式如下图所示,则下列有关说法中正确的是( )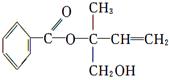
| A.X的分子式为C12H16O3 |
| B.X在一定条件下能发生加成、加聚、取代、消去等反应 |
| C.在Ni作催化剂的条件下,1 mol X最多只能与1 mol H2加成 |
| D.可用酸性高锰酸钾溶液区分苯和X |
下列有关说法正确的是
| A.反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H<0 |
| B.高温下,工业上用纯碱和石英砂制玻璃,说明硅酸的酸性强于碳酸 |
| C.加热蒸干氯化铝溶液并灼烧残留物至质量不变,所得固体为氧化铝 |
| D.高温下,用金属钠与氯化钾可以置换出金属钾,说明钠的金属性比钾强 |
短周期主族元素A、B、C、D、E的原子序数依次增大,其中只有C是金属元素,B是地壳中含量最多的元素,A元素常见化合价为+1和-1;A与C的最外层电子数相同,C、D两元素原子的电子数之和为A、B两种元素原子的电子数之和的3倍。下列叙述正确的是()
A.元素的原子半径:A<B<C< D< E
B.对应氢化物的热稳定性:D > E
C.B与C、B与D形成的化合物中化学键类型相同
D.五种元素中最高价氧化物对应的水化物酸性最强的是E
实验室可用NaNO2+NH4Cl==NaCl+N2↑+2H2O制备N2,下列说法正确的是()
| A.NaNO2发生氧化反应 | B.NH4Cl中的氮元素被还原 |
| C.N2既是氧化产物,又是还原产物 | D.每生成1mol N2转移电子的物质的量为6mol |