准确移取20.00mL某待测HCl溶液于锥形瓶中,用0.1000mol·L-1NaOH溶液滴定,下列说法正确的是
| A.滴定管用蒸馏水洗涤后,装入NaOH溶液进行滴定 |
| B.随着NaOH溶液滴入,锥形瓶中溶液pH由小变大 |
| C.用酚酞作指示剂,当锥形瓶中溶液由红色变无色时停止滴定 |
| D.滴定达终点时,发现滴定管尖嘴部分有悬滴,则测定结果偏小 |
参照反应Br+H2 HBr+H的能量对应反应历程的示意图,下列叙述中正确的是()
HBr+H的能量对应反应历程的示意图,下列叙述中正确的是()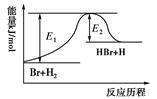
| A.正反应为吸热反应 |
| B.吸热反应一定要加热后才能发生 |
| C.反应物总能量高于生成物总能量 |
| D.升高温度可增大正反应速率,降低逆反应速率 |
随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是()
| A.利用电池外壳的金属材料 |
| B.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 |
| C.防止电池中渗漏的电解质溶液腐蚀其他物品 |
| D.回收其中的石墨电极 |
下列属于吸热反应的是()
| A.金属钠与水的反应 | B.氢气燃烧 |
| C.浓硫酸的稀释 | D.Ba(OH)2·8H2O和NH4Cl(固体)混合 |
X、Y是元素周期表ⅦA族中的两种元素。下列叙述中不能说明X的非金属性比Y强的是
| A.X原子的电子层数比Y原子的电子层数少 |
| B.酸性:HXO4>HYO4 |
| C.X的气态氢化物比Y的气态氢化物稳定 |
| D.Y的单质能将X从NaX的溶液中置换出来 |
下列关于有机化合物的认识不正确的是()
| A.油脂在空气中完全燃烧转化为水和二氧化碳 |
| B.蔗糖、麦芽糖的分子式都是C12H22O11,二者互为同分异构体 |
| C.在水溶液里,乙酸分子中的—CH3可以电离出H+ |
| D.在浓硫酸存在下,苯与浓硝酸共热生成硝基苯的反应属于取代反应 |