[化学——选修3:物质结构与性质]
决定物质性质的重要因素是物质结构。请回答下列问题。
(1)+3价Cr的配合物K[Cr(C2O4)2(H2O)2]中,配体是___________,与C2O42-互为等电子体的分子是(填化学式)_______________。

(2)CaO晶胞如图所示,与每一个钙离子距离最近并且距离相等的钙离子有_________个 ;CaO晶体和NaCl晶体的晶格能分别为:CaO:3401 kJ/mol、NaCl:786 kJ/mol。 导致两者晶格能差异的主要原因__________________。
(3)Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g)反应过程中,断裂的化学键类型是__________,则形成的化学键类型是 。
(4)从不同角度观察MoS2的晶体结构见图。已知:Mo位于第五周 期VIB族。
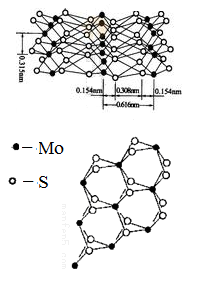
①下列说法正确的是__________
| A.晶体硅中硅原子的轨道杂化类型为sp2 |
| B.电负性:C<S |
| C.晶体硅和C60比较,熔点较高的是C60 |
| D.Mo元素基态原子的价电子排布式为4d55s1 |
E.MoS2的晶体中每个Mo原子周围距离最近的S原子数目为4
F.MoS2的晶体中Mo-S之间的化学键为极性键、配位键、范德华力
②根据MoS2的晶体结构回答:MoS2纳米粒子具有优异的润滑性能,其原因是_____________ .
在6份0.01 mol·L-1氨水中分别加入下列各物质:
| A.浓氨水 | B.纯水 |
| C.少量K2CO3固体 | D.少量浓H2SO4 |
E.少量NaOH固体 F.少量Al2(SO4)3固体
(1)能使c(OH-)减小、c(NH4+)增大的是;
(2)能使(OH-)增大、c(NH4+)减小的是;
(3)能使c(OH-)和c(NH4+)都增大的是;
(4)能使c(OH-)和c(NH4+)都减小的是。
(1)键线式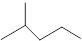 表示的分子式;名称是。
表示的分子式;名称是。
(2)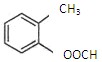 中含有的官能团的名称为。与其含有相同官能团,且分子结构中苯环上只有一个取代基的同分异构体有种。写出它们的结构简式。
中含有的官能团的名称为。与其含有相同官能团,且分子结构中苯环上只有一个取代基的同分异构体有种。写出它们的结构简式。
X、Y、Z、W、Q、R六种短周期主族元素,原子序数依次增大,Z基态原子核外有三个未成对电子,Y、Z、W分别与X形成常见化合物的分子结构依次为正四面体、三角锥形和V形,Q的各级电离能如下表,W与R是同族元素。
| Q |
I1 |
I2 |
I3 |
I4 |
I5 |
… |
| 电离能(kJ/mol) |
496 |
4562 |
6912 |
9543 |
13353 |
… |
回答下列有关问题:
(1)W原子的外围电子排布图为_______________________________。
(2)化合物Q2W2的电子式______________,化合物XYZ的结构式________________。
(3)相同条件下,YW2、RW2两者在水中的溶解度较大的是(写分子式),原因是。
(4)RW3分子中的键角___________,RW32-分子的立体构型是_______________形。
(5)Y、W、Q三种元素所形成的常见化合物的晶体类型为,YW2中的化学键类型为共价键(填“极性”或“非极性”),根据等电子原理,指出与YW互为等电子体且含有Z原子的微粒有(要求写一种即可)。
下表为周期表的一部分,表中所列的字母分别代表一种化学元素。
| a |
|||||||||||||||||
| b |
c |
d |
|||||||||||||||
| e |
f |
||||||||||||||||
| g |
h |
||||||||||||||||
用化学用语回答下列问题:
(1)写出元素g的基态原子核外电子排布式___________________________,
h2+中未成对电子数为。
(2)在b2a2分子中,元素b为杂化,该分子是分子(填“极性”或“非极性”),该分子中σ键和π键的数目比为。
(3) bd2与bf2比较,沸点较高的是_______(填分子式),原因是。
(4)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙正确是。
A.h位于元素周期表中第四周期第VIII族,属于d区元素
B.e的基态原子中,3p能级为半充满,属于p区元素
C.最外层电子排布式为4s2,一定属于IIA族
D.最外层电子排布式为ns2np1,该元素可能是ⅢA族或ⅢB族
(5)科学研究表明,元素b与元素c可以形成一种超硬、耐磨、耐高温的新型无机非金属材料,其化学式为,其熔点比金刚石(填“高”或“低”)。
钛(Ti)被誉为“21世纪的金属”。工业上将TiO2与焦炭混合,通入Cl2高温下制得TiCl4;再将TiCl4提纯后,在氩气保护下与镁高温反应制得Ti。其反应如下:
①TiO2+2Cl2+2C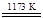 TiCl4+2CO②TiCl4+2Mg
TiCl4+2CO②TiCl4+2Mg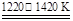 Ti+2MgCl2
Ti+2MgCl2
回答下列问题:
(1)已知TiCl4在通常情况下是无色液体,熔点为–37℃,沸点为136℃;TiCl4在潮湿空气中易水解产生白雾,同时产生H2TiO3固体。
① TiCl4为______晶体(填“离子”、“原子”或“分子”)。
② TiCl4分子为正四面体形,则Ti为________杂化。
③ TiCl4在潮湿空气中水解的化学方程式是_________________________________。
(2)配离子[TiCl(H2O)5]2+的中心离子化合价为 ,中心离子配位数为 。