下列事实不能用平衡移动原理解释的是
| A.配制FeCl3溶液时加入少量的浓盐酸 |
| B.常温下,NaOH溶液中由水电离出的c(H+)<1×10-7mol/L |
| C.AgCl在水中的溶解度大于在饱和NaCl溶液中的溶解度 |
| D.工业上SO2转化为SO3用五氧化二钒铁触媒作为催化剂 |
下列判断错误的是
| A. |
沸点: |
B. |
熔点: |
| C. |
酸性: |
D. |
碱性: |
一定条件下磷与干燥氯气反应,若0.25 磷消耗掉314 氯气(标准状况),则产物中 与 的物质的量之比接近于
| A. | 1:2 | B. | 2:3 | C. | 3:1 | D. | 5:3 |
下图表示4-溴环己烯所发生的4个不同反应。其中,产物只含有一种官能团的反应是
| A. | ①④ | B. | ③④ | C. | ②③  |
D. | ①② |
下面关于SiO2晶体网状结构的叙述正确的是
| A.存在四面体结构单元,O处于中心,Si处于4个顶角 |
| B.最小的环上,有3个Si原子和3个O原子 |
| C.最小的环上,Si和O原子数之比为1:2 |
| D.最小的环上,有6个Si原子和6个O原子 |
下列叙述正确的是
A.在醋酸溶液的 ,将此溶液稀释1倍后,溶液的 ,将此溶液稀释1倍后,溶液的 ,则 ,则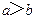 |
B.在滴有酚酞溶液的氨水里,加入 至溶液恰好无色,则此时溶液的 至溶液恰好无色,则此时溶液的 |
C.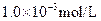 盐酸的 盐酸的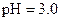 , , 盐酸的 盐酸的 |
D.若1mL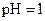 的盐酸与100mL 的盐酸与100mL 溶液混合后,溶液的 溶液混合后,溶液的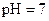 则 则 溶液的 溶液的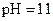 |