某温度时,N2与H2反应过程中的能量变化如图所示。下列叙述正确的是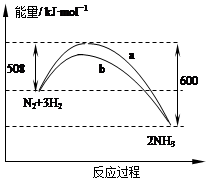
| A.a曲线是加入催化剂时的能量变化曲线 |
| B.在密闭容器中加入1 mol N2、3 mol H2,充分反应放出的热量小于92 kJ |
| C.由图可知,断开1mol 氮氮三键与1 mol 氢氢键吸收的能量和小于形成1mol 氮氢键所放出的能量 |
| D.反应物的总能量低于生成物的能量 |
在C(s)+CO2(g)===2CO(g)的反应中,现采取下列措施:
①缩小体积,增大压强②增加碳的量 ③通入CO2④恒容下充入N2⑤恒压下充入N2能够使反应速率增大的措施是
| A.①④ | B.②③⑤ | C.①③ | D.①②④ |
反应4A(g)+3B(g) 2C(g)+D(g),经2min,B的浓度减少0.6 mol•L-1。对此反应速率的表示,正确的是
2C(g)+D(g),经2min,B的浓度减少0.6 mol•L-1。对此反应速率的表示,正确的是
①用A表示的反应速率是0.4 mol•L-1•min-1
②分别用B、C、D表示的反应速率其比值为3:2:1
③在2 min末的反应速率,用B表示是0.3 mol•L-1•min-1
④在这2 min内用B表示的反应速率的值是逐渐减小的,用C表示的反应速率的值是逐渐增大的
A. ①② B.③ C.① D. ②④
在一定温度下,容器内某一反应中M、N的物质的量随反应时间的变化曲线如图,下列表述中正确的是
A.反应的化学方程式为:2M N N |
B.t2时,正逆反应速率相等,达到平衡 |
| C.t3时,正反应速率大于逆反应速率 | D.t1时,N的浓度是M浓度的2倍 |
从下列实验事实所引出的相应结论正确的是
| 选项 |
实验事实 |
结论 |
| A |
其他条件相同,Na2S2O3溶液浓度越大,析出硫沉淀所需时间越短 |
当其他条件不变时,增大反应物浓度化学反应速率加快 |
| B |
在化学反应前后,催化剂的质量和化学性质都没有发生改变 |
催化剂一定不参与化学反应 |
| C |
物质的量浓度相同的盐酸和醋酸分别与等质量的形状相同的锌粒反应 |
反应开始速率相同 |
| D |
在容积可变的密闭容器中发生反应 H2(g)+I2(g)  2HI(g),把容积缩小一倍 2HI(g),把容积缩小一倍 |
正反应速率加快,逆反应速率不变 |
在密闭容器中,进行可逆反应,A与B反应生成C,其反应速率分别为v1、v2、v3(单位:mol·L-1·s-1),且v1、v2、v3之间有如下关系:3v1=v2,2v1=v3,2v2=3v3,则此反应表示为
A.A+B C C |
B.2A+2B 3C 3C |
C.3A+B 2C 2C |
D.A+3B 2C 2C |