【化学选修3—物质结构与性质】A、B、C、D、E、F、G为原子序数依次增大的前四周期元素。A、F原子的最外层电子数均等于其周期序数.F原子的电子层数是A的3倍; B原子核外电子分处3个不同能级。且每个能级上排布的电子数相同;A与C形成的最简单分子为三角锥形;D原子p轨道上成对电子数等于未成对电子数;E原子核外每个原子轨道上的电子都已成对.E与F同周期;G的原子序数等于A、C、D、F 四种元素原子序数之和。
(1)写出B的基态原子的核外电子排布图 ;回答E与F原子的第一电离能的大小关系怎样,原因是 ;
(2)C3-是一种弱酸根离子,请写出两种与C3-互为等电子体的分子的化学式 , ;
(3)A与D形成的A2D2分子中D原子的杂化类型为 杂化,A与C形成的最简单分子易溶于水的原因 ;
(4)G的晶体中原子按 (填“ABABAB”或“ABCABCABC”)的方式堆积而成,G的晶体堆积模型名称 ;
(5)G的晶体中G原子的配位数为 ,空间利用率为 ;
(6)元素G的一种氯化物的晶胞如图所示,该氯化物的化学式 ,两种微粒间最短距离为460.0 pm,晶体密度为 g/cm3。(列式表示)

在一定条件下相互转化关系如图所示(反应条件和部分产物已省略)
(1)若A为金属单质,B、C为常温下气态非金属单质,D为黑色晶体,A和E在一定条件下反应生成D的化学方程式为.
(2)若A为金属单质,B、C为非金属单质,C为黑色固体,A和E在一定条件下反应生成D的化学方程式为.
(3)若A为非金属单质,B为金属单质,C为D的水溶液,图示中所有反应均为化合反应,A和E在水溶液中反应生成D的离子方程式为____________________________,B和C在水溶液中反应生成E的离子方程式为_______________________________________。
A是一种红棕色金属氧化物,B、D是常见金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解。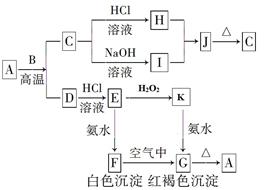
按要求写方程式:
(1)A与B在高温条件下生成C和D的化学方程式:_________________________
(2)F在空气中转化为G的化学方程式:___________________________________
(3)C转化为I的离子方程式:_______________________________________
(4)E转化为K的离子方程式:______________________________________
(13分)下图的各方框表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A、C、D为无色气体,C能使湿润的红色石蕊试纸变蓝。
(1)写出下列各物质的化学式:
X:;B:;F:;G:。
(2)写出下列变化的反应方程式:
A→D:;G→E:。
(3)实验室里,常用加热的混合物的方法制取气体C,常采用法来收集,可否用无水CaCl2干燥气体C (填“否”或者“可以”)。
某工程塑料PBT的结构简式为
其合成路线如下:
试回答下列问题:
(1)A的系统命名为:,它与 互为 关系。
互为 关系。
(2)指出反应类型:A→B:,B→C:。
(3)B的结构简式(或键线式)为:。它(填“有”或“无”)顺反异构体。
(4)写出D+E→PBT的化学方程式:。
已知A是一种常见金属,F是一种红褐色沉淀。试根据图中转化关系,回答下列问题。
(1)写出A、C、F、G的化学式:A,C,F,G。
(2)检验D中阳离子的方法。
(3)保存C溶液时为什么要加固体A。
(4)写出下列转化的离子方程式C→D:。