汽车尾气中,产生NO的反应为:N2(g)+O2(g) 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化。下列叙述正确的是
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化。下列叙述正确的是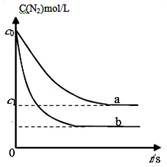
A.温度T下,该反应的平衡常数K= 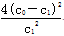 |
| B.温度T下,随着反应的进行,混合气体的密度减小 |
| C.曲线b对应的条件改变可能是加入了催化剂 |
| D.若曲线b对应的条件改变是温度,可判断该反应的△H<0 |
阿伏加德罗常数约为6.02×1023mol-1,下列说法中正确的是()
| A.22.4LH2含氢分子数为6.02×1023 |
| B.32gO2中含有的氧原子数为2×6.02×1023 |
| C.0.1mol/L NaCl溶液中,含Na+的数目为6.02×1022 |
| D.标准状况下,22.4L H2O含水分子数为6.02×1023 |
下列有关碳酸钠、碳酸氢钠的说法中,正确的是()
| A.除去碳酸钠固体中混有的少量碳酸氢钠可以采用加热的方法 |
| B.相同条件下,碳酸钠的溶解度小于碳酸氢钠的溶解度 |
| C.碳酸钠与盐酸反应放出二氧化碳的剧烈程度强于碳酸氢钠 |
| D.向碳酸钠溶液和碳酸氢钠溶液中滴加少量酚酞试液,都不显红色 |
下列溶液中的氯离子浓度与100mL 0.5 mol•L―1氯化铝溶液中的氯离子浓度相等的是( )
| A.50mL 1.5 mol•L―1的KCl溶液 | B.50mL 0.5 mol•L―1的FeCl2溶液 |
| C.100mL 1 mol•L―1的MgCl2溶液 | D.450mL 0.5 mol•L―1的NaCl溶液 |
吸入人体內的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体內的活性氧,由此推断Na2SeO3的作用是()
A作还原剂 B作氧化剂
C既作氧化剂又作还原剂 D既不作氧化剂又不作还原剂
下列各组离子能在溶液中大量共存的是( )
| A.H+、Ba2+、NO3-、OH- | B.Mg2+、Na+、Cl-、OH- |
| C.Na+、H+、NO3-、CO32- | D.Cu2+、Fe3+、Cl-、SO42- |