下列说法不正确的是
| A |
B |
C |
D |
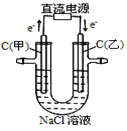
| 通电一段时间后, 搅拌均匀,溶液的 pH增大 |
甲电极上的电极反应为: 2Cl--2e-= Cl2↑ |
Pt电极上的电极反应为: O2+2H2O+4e-==4OH- |
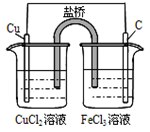
总反应的离子方程式 为:2Fe3++Cu=Cu2++ 2Fe2+ |
 |
 |
 |
 |
下列有关实验原理或实验操作正确的是
| A.将氯化铁固体溶于稀盐酸配制FeCl3溶液 |
| B.称取4.0gNaOH,放入100mL容量瓶中,加水稀释,配制1.0mol·L-1的NaOH溶液 |
| C.利用图1装置定量测定H2O2的分解速率 |
| D.如图2所示,关闭弹簧夹检查装置的气密性 |
常温下,下列各组离子一定能在指定溶液中大量共存的是
| A.使甲基橙呈红色的溶液:Na+、NH4+、AlO2-、CO32- |
| B.8% H2O2溶液:H+、Fe2+、SO42-、Cl- |
| C.含有Fe3+的溶液:Na+、Al3+、Cl-、SCN- |
| D.Kw/c(H+)=0.1 mol·L-1的溶液:Na+、K+、CO32-、ClO- |
原子序数依次增大的短周期主族元素X、Y、Z、W,X是最外层只有一个电子的非金属元素,Y是地壳中含量最高的元素,W的原子序数是Y的2倍,X、Y、Z、W最外层电子数之和为15。下列说法正确的是
| A.X和Y只能形成一种化合物 | B.简单离子半径:W2->Y2->Z2+ |
| C.简单气态氢化物的热稳定性:W>Y | D.WY2、ZY中化学键类型相同 |
Mg和SiO2在高温下反应生成MgO和Mg2Si。下列说法正确的是
| A.微粒的半径:Si > Mg | B.氧元素不存在同素异形体 |
| C.Mg的还原性强于Si | D.该反应是置换反应,镁元素被氧化 |
下列说法正确的是
| A.在化学反应中,原子重新组合时伴随着能量的变化 |
| B.淀粉和纤维素的化学式均为(C6H10O5)n,故互为同分异构体 |
| C.通过化学变化可以“点石成金”,即可将黏土转化成金单质 |
| D.等质量的铝粉按a、b两种途径完全转化,途径a比途径b消耗更多的NaOH |
