下表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断以下叙述正确的是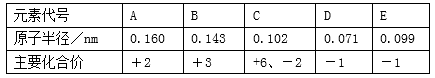
A.A、B的单质与稀盐酸反应速率B>A
B.D、E形成的简单离子的还原性E->D-
C.气态氢化物的稳定性HD<H2C
D.最高价氧化物对应的水化物的酸性 H2CO4>HEO4
X、Y是元素周期表Ⅶ族中的两种元素.下列叙述中能说明X的非金属性比Y强的是
| A.X原子的电子层数比Y原子的电子层数多 |
| B.X的氢化物的沸点比Y的氢化物的沸点低 |
| C.X的气态氢化物比Y的气态氢化物稳定 |
| D.Y的单质能将X从NaX的溶液中置换出来 |
下列溶液与100mL0.5mol/LNa2SO4溶液中的 Na+的物质的量浓度相等的是
| A.200mL0.5mol/LNaCl溶液 | B.100mL1mol/LNa2CO3溶液 |
| C.100mL0.5mol/LNa3PO4溶液 | D.1L1mol/LNaOH溶液 |
在恒容密闭容器中进行的反应:2CO2(g)+6H2(g) C2H5OH(g)+3H2O(g) △H 。在某压强下起始时按不同氢碳比[n(H2)/n(CO2)]投料(见右图中曲线①②③),测得CO2的平衡转化率与温度关系如下图所示,
C2H5OH(g)+3H2O(g) △H 。在某压强下起始时按不同氢碳比[n(H2)/n(CO2)]投料(见右图中曲线①②③),测得CO2的平衡转化率与温度关系如下图所示,
下列有关说法正确的是
| A.该反应:△H >0 |
| B.氢碳比:①<②<③ |
| C.其它条件不变的情况下,缩小容器的体积可提高CO2的转化率 |
| D.若起始CO2浓度为2mol·L-1、H2为4mol·L-1,在图中曲线③氢碳比条件下进行,则400K时该反应的平衡常数数值约为1.7 |
25℃时,0.1mol·L-1下列溶液的pH如下表,有关比较错误的是
| 序号 |
① |
② |
③ |
④ |
| 溶液 |
NaCl |
CH3COONH4 |
NaF |
NaHCO3 |
| pH |
7.0 |
7.0 |
8.1 |
8.4 |
A.酸的强度:HF>H2CO3
B.由水电离产生的c(H+):①=②
C.溶液中酸根离子浓度:c(F-)>c(HCO3-)
D.序号④中:c(HCO3-)+c(CO32-)+c(H2CO3)=0.1mol·L-1
在探究常见物质成分的实验中,下列根据实验现象得出的结论正确的是